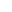- 手机:13761418683
电话:021-38015121
联系人:Absin
邮箱:zhouzz@univ-bio.com
网址:http://www.absin.cn/
地 址:上海市浦东新区新浩路58号18号楼

- 1. 肿瘤细胞依赖多胺代谢维持增殖,靶向该通路可能增强 KRAS 抑制剂敏感性;
- 2. KEAP1 突变状态可能影响多胺代谢关键酶表达,进而决定治疗响应;
- 3. 多胺代谢与铁死亡存在调控关联,可通过该通路放大抗癌效应。
- 在 KRAS^MU/KEAP1^WT 细胞、类器官及动物模型中,补充精胺、亚精胺等多胺可直接增强 KRAS 抑制剂疗效(图 1H-K);
- 而 KRAS^MU/KEAP1^MU 模型需先通过慢病毒 / AAV 介导 SAT1 过表达,再联合多胺治疗才能有效致敏(图 6C-D)。
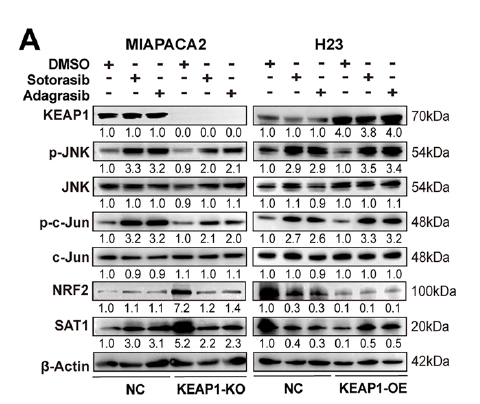
- KEAP1^WT 细胞中,KRAS 抑制剂通过 JNK/c-Jun 通路激活 SAT1,促进多胺分解产生活性氧(ROS),诱导铁死亡(图 5A);
- KEAP1^MU 细胞中,JNK 通路加速 NRF2 降解,抑制 SAT1 表达,需外源性过表达 SAT1 恢复致敏效应(图 2H)。
靶向 SAT1 - 多胺代谢铁死亡通路:突破 KRAS 靶向治疗耐药的精准抗癌新策略
2026-03-31
在肿瘤治疗领域,KRAS 突变癌症因耐药性问题一直是临床难题,而 KEAP1 共突变更是让治疗效果雪上加霜。近期《Nature Communications》发表的重磅研究,揭示了基于 KEAP1 状态的精准治疗新策略 —— 靶向 SAT1 介导的多胺代谢与铁死亡,可显著增强 KRAS 靶向治疗疗效。Absin 类器官培养试剂盒在研究中发挥关键作用,助力科研团队完成核心实验验证。
文献标题:Targeting polyamine metabolism and ferroptosis enhances the efficacy of KRAS-targeted therapy depending on KEAP1 status
发表期刊:Nature Communications(IF 15.7)
DOI:https://doi.org/10.1038/s41467-025-65441-4
使用 Absin 试剂:Organotial 人肺癌类器官培养试剂盒(abs9443)

一、研究核心思路:锁定代谢靶点,破解耐药困局
KRAS 突变在胰腺癌、结直肠癌、肺癌中高发,尽管 sotorasib 等靶向药已获批上市,但 KEAP1 等基因共突变导致的耐药性严重限制临床获益。研究团队从 "代谢重编程 + 铁死亡调控" 双角度切入,提出核心假设:
研究通过 "代谢库筛选→细胞 / 类器官验证→机制解析→动物模型确认" 的层层递进思路,最终阐明 KRAS-KEAP1-SAT1-铁死亡的调控网络,为精准治疗提供新方向。
二、关键研究成果:分状态治疗,疗效翻倍
1. 多胺增效具有 KEAP1 依赖性
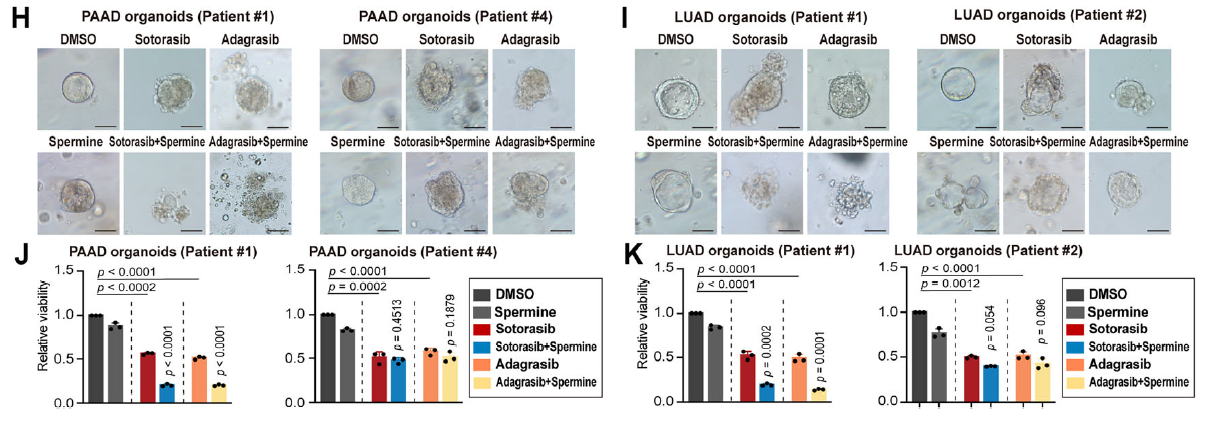
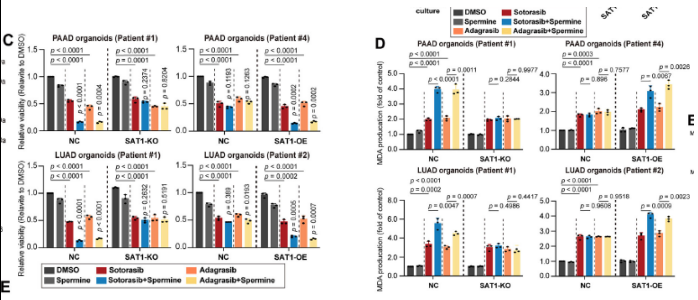
2. SAT1 是核心调控节点
SAT1 作为多胺分解代谢关键酶,其表达受 KEAP1 状态调控:
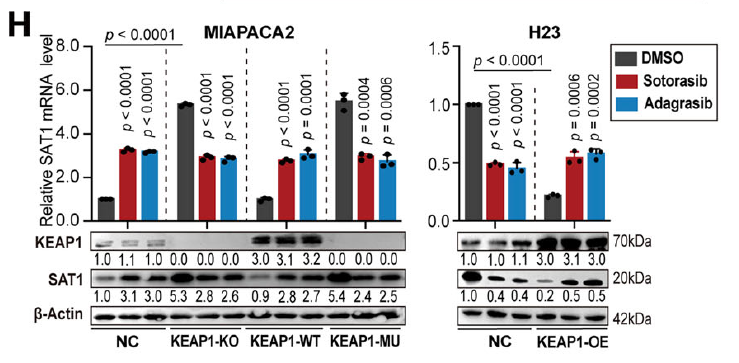
3. 突破耐药屏障
在长期诱导的 KRAS 抑制剂耐药细胞中,多胺 + SAT1 靶向策略仍能通过促进脂质过氧化、升高 MDA 水平等铁死亡特征,恢复药物敏感性(图 4H),为临床耐药后治疗提供新方案。
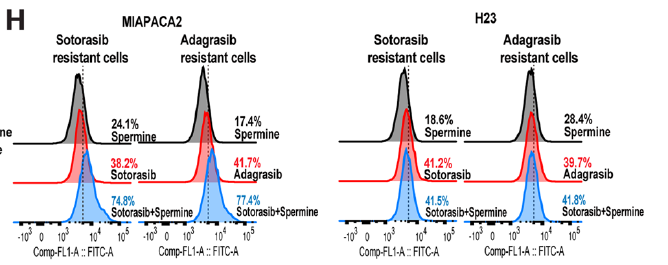
三、Absin 产品助力:关键实验的核心工具支撑
研究中,Absin 的 PDO 培养相关产品为类器官模型构建提供了关键支持,具体信息如下:
| 产品名称 | 货号 | 应用场景 | 核心作用 |
|---|---|---|---|
| Organotial人肺癌类器官培养试剂盒 | abs9443 | 从 KRAS 突变胰腺癌(PAAD)、肺癌(LUAD)患者肿瘤组织中构建患者来源类器官(PDO)(图 1F-G) |
1. 提供类器官生长所需的特异性营养成分,维持肿瘤组织原代细胞的三维结构与异质性; 2. 保障 PDO 在体外稳定培养,成功用于多胺 + KRAS 抑制剂的协同效应验证; 3. 支持类器官中 SAT1 基因敲除 / 过表达后的功能验证实验,为临床转化提供可靠的体外模型。 |
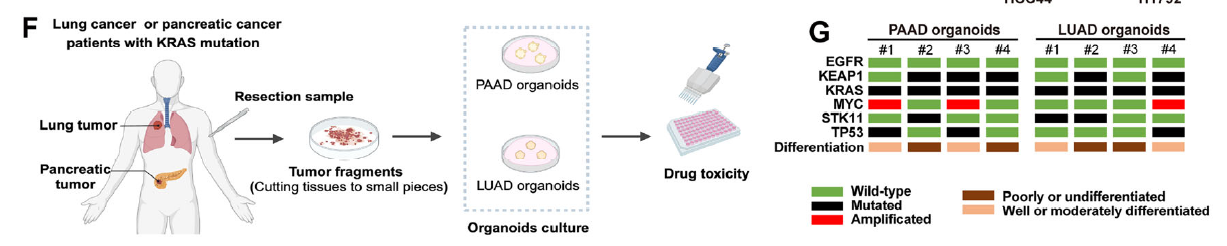
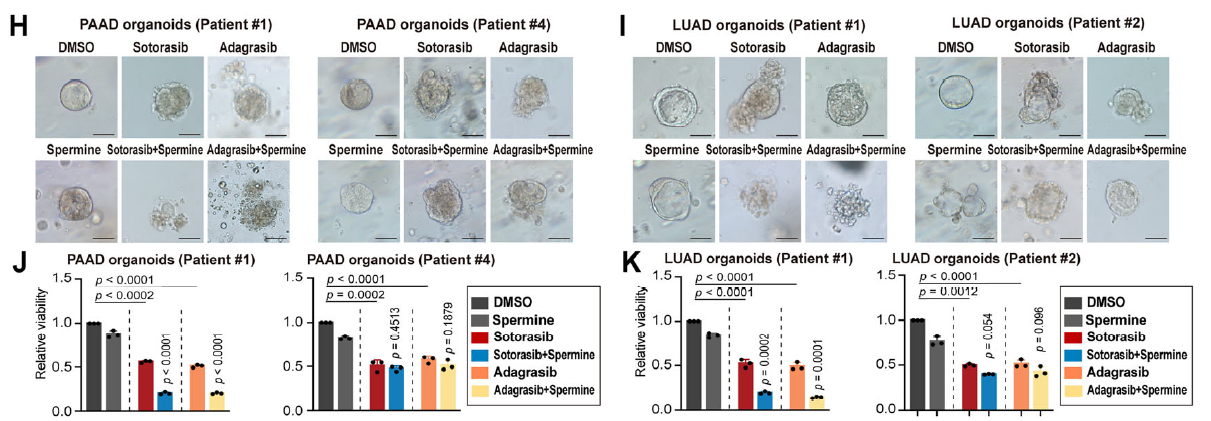
类器官模型因能精准模拟体内肿瘤微环境,已成为精准医疗研究的核心工具。Absin 的 PDO 培养试剂盒凭借优异的稳定性和兼容性,助力研究团队高效完成从临床样本到实验模型的转化,为 "多胺增效策略" 的临床适用性验证奠定了基础。
四、研究意义与展望
该研究首次揭示 KEAP1 状态对多胺代谢靶向治疗的决定性作用,提出 "KRAS 抑制剂 + 多胺补充(KEAP1 野生型)" 和 "SAT1 过表达 + 多胺补充 + KRAS 抑制剂(KEAP1 突变型)" 的分层治疗方案,为 KRAS 突变癌症的精准治疗提供新范式。
本文内容基于《Nature Communications》(DOI: 10.1038/s41467-025-65441-4)原文献;文中涉及的原文献图片、数据等知识产权归原期刊及研究团队所有。若存在侵权情形,敬请及时联系我方删除,我方将积极配合处理。