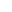- 手机:13761418683
电话:021-38015121
联系人:Absin
邮箱:zhouzz@univ-bio.com
网址:http://www.absin.cn/
地 址:上海市浦东新区新浩路58号18号楼

- 优化载体组成:构建包含阳离子脂质(DOTMA/DOTAP)、可电离脂质(MC3/ALC0315/SM102)、辅助脂质(DOPE)、胆固醇和 PEG - 脂质的五组分 LNPs,通过调节各成分比例,平衡蛋白结合能力与内体逃逸效率;
- 解决血清稳定性难题:利用 PEG 修饰减少血清蛋白非特异性吸附,同时借助血清白蛋白的受体介导内吞途径,提升体内递送效率;
- 聚焦临床转化:选择肿瘤治疗中具有重要价值的蛋白(皂素 saporin、白细胞介素 IL-10 等),验证 LNPs 在体外细胞、3D 肿瘤球和体内动物模型中的递送效果与治疗潜力。
- 体外实验:验证 LNPs 对细胞因子的封装效率与活性保持能力;
- 体内实验:构建 IL-10-LNPs 制剂,通过静脉注射递送,评估其在黑色素瘤模型中增强过继性 T 细胞治疗的效果。
- 作为功能明确的免疫调节分子,Absin 重组小鼠 IL-10 为 LNPs 的体内递送效果提供了直接的功能读出指标 —— 通过检测肿瘤组织中 IL-10 浓度、T 细胞增殖及细胞因子分泌水平,清晰验证了 LNPs 的体内递送效率与靶向性;
- 凭借高纯度、高生物活性的产品特性,确保了实验结果的可靠性与重复性,为 “LNPs 延长细胞因子半衰期、增强免疫治疗效果” 这一核心结论提供了坚实支撑。
突破蛋白递送瓶颈,脂质纳米颗粒(LNPs)赋能癌症免疫治疗
2026-04-01
在生物制药领域,蛋白类治疗药物凭借高活性、高特异性的优势,成为癌症、自身免疫性疾病等重大疾病治疗的核心方向。然而,蛋白药物的胞内递送始终面临着封装效率低、内体逃逸难、血清稳定性差等多重挑战,严重限制了其临床应用潜力。近日,一项发表于《Advanced Science》的重磅研究(DOI: 10.1002/advs.202500844)成功破解了这一难题 —— 研究团队设计了一种新型五组分脂质纳米颗粒(LNPs),实现了多种蛋白药物的高效胞内递送,为癌症免疫治疗带来了革命性突破。该研究中,Absin的重组小鼠IL-10蛋白作为关键的实验材料,为验证LNPs的递送效能提供了重要依据。
文献标题:Optimization of Lipid Nanoparticles with Robust Efficiency for the Delivery of Protein Therapeutics to Augment Cancer Immunotherapy
发表期刊:Advanced Science(IF 14.1)
DOI:https://doi.org/10.1002/advs.202500844
使用 Absin 产品:Mouse recombinant IL-10


一、研究思路:精准破解蛋白递送的三重核心障碍
传统 LNPs 在核酸递送(如 mRNA 疫苗)中已展现出强大实力,但在蛋白递送中却屡屡受限。究其原因,蛋白的电荷异质性、结构复杂性与核酸差异显著,导致载体结合难、内体逃逸效率低、血清中易失活。为此,研究团队提出了 “阳离子脂质 + 可电离脂质” 的协同设计思路:
二、核心研究成果:从高效递送到癌症治疗的全链条突破
1. 多类型蛋白的高效胞内递送,活性保持率优异
优化后的 LNPs(DOTMA/MC3/DOPE 摩尔比 20:20:20)对不同分子量、等电点的蛋白均表现出强大递送能力,包括抗体(IgG)、酶(SOD、CAT)、毒素(saporin)、Cas9 核糖核蛋白等(图 4)。其中,GFP 蛋白的细胞阳性率超过 80%,显著优于商用试剂 Pulsin,且递送的蛋白能保持天然生物活性 —— 如 SOD 可有效清除细胞内活性氧(ROS),Cas9 RNP 能成功实现基因组编辑(图 4f)。
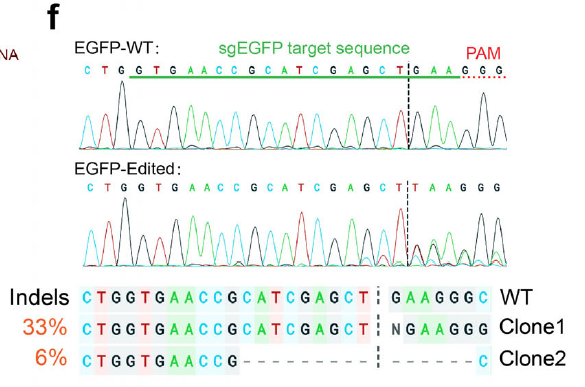
2. 血清增强型递送机制,体内靶向性突出
研究发现,LNPs 表面可吸附血清白蛋白,通过白蛋白受体介导的小窝蛋白依赖内吞途径进入细胞(图 3),这一机制不仅提升了血清环境下的递送效率,还借助肿瘤细胞高表达白蛋白受体的特性,实现了肿瘤组织的靶向富集。在 3D 肿瘤球模型中,Cy5.5 标记的皂素 - LNPs 能高效穿透肿瘤组织,而游离皂素几乎无法渗透(图 5d)。
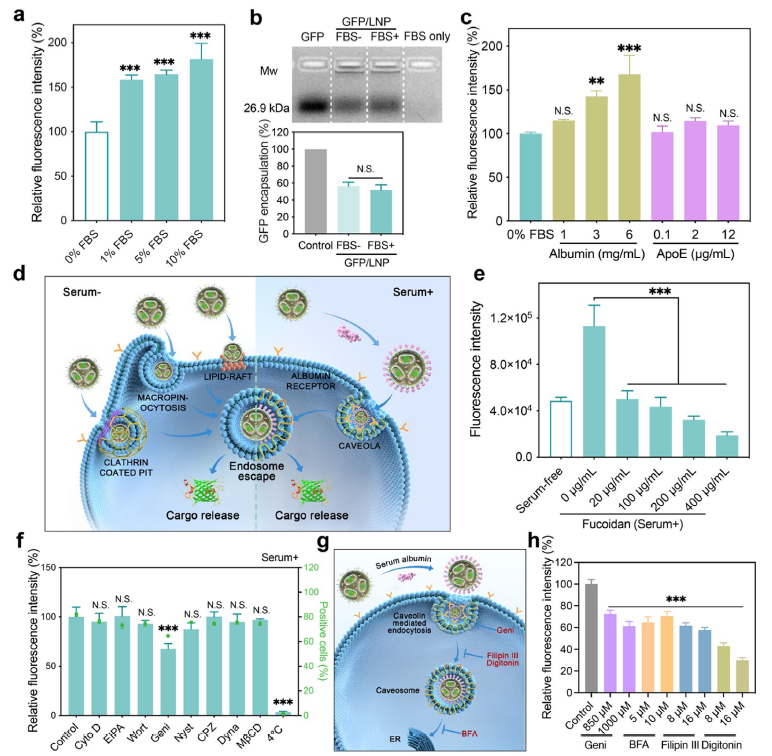
LNPs 的血清耐受机制与细胞内转运路径(原文 Figure 3)

皂素 - LNPs 的 3D 肿瘤球穿透效果(原文 Figure 5d)
3. 癌症治疗的重大突破:IL-10 递送增强免疫治疗效果
在黑色素瘤模型中,研究团队验证了 IL-10-LNPs 的免疫治疗潜力:IL-10 作为关键细胞因子,可缓解 T 细胞耗竭、促进其增殖与细胞毒性。通过 LNPs 递送 IL-10,不仅延长了 IL-10 的体内半衰期,还显著提升了肿瘤组织中 IL-10 浓度,与过继性 OT-1 CD8+ T 细胞联合使用时,肿瘤生长抑制率大幅提高,小鼠生存期显著延长(图 6)。流式细胞分析显示,治疗后肿瘤浸润的 CD3+ T 细胞和 OT-1 CD8+ T 细胞数量显著增加,且 IFN-γ 分泌水平升高,证明免疫应答被有效激活。
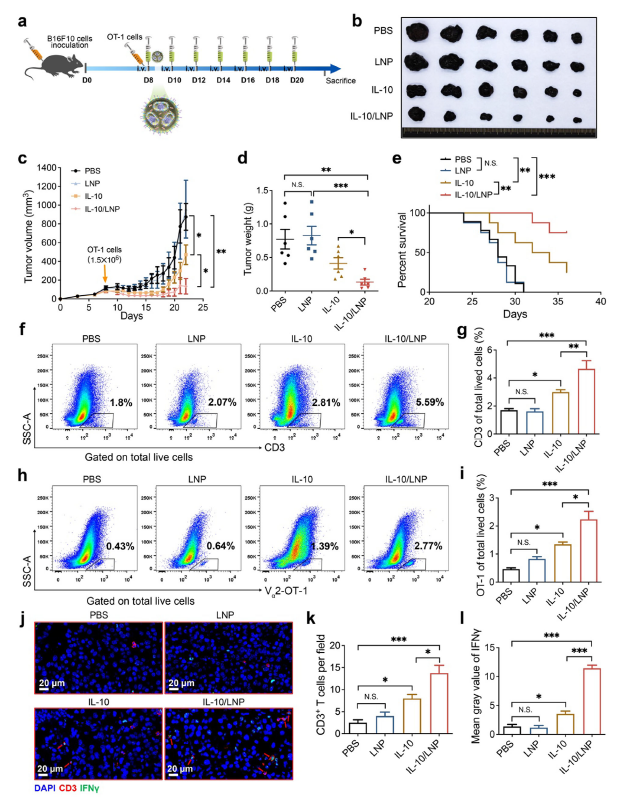
IL-10-LNPs 联合过继性 T 细胞治疗黑色素瘤的效果(原文 Figure 6)
三、Absin 产品助力:重组小鼠 IL-10 成为免疫治疗验证的关键
在这项里程碑式的研究中,Absin 重组小鼠 IL-10 贯穿了体内外免疫治疗效果验证的关键环节:
1. 产品应用场景:
2. 发挥的核心作用:
| 产品名称 | 应用场景 | 核心作用 |
|---|---|---|
| Mouse recombinant IL-10 | 体外封装效率验证、体内免疫治疗实验 | 功能读出指标、确保实验可靠性与重复性 |
四、总结与展望
该研究通过巧妙的载体设计,成功突破了蛋白药物胞内递送的技术瓶颈,拓展了 LNPs 在生物大分子递送中的应用边界,尤其为细胞因子、毒素蛋白等难以递送的治疗分子提供了高效载体平台。Absin 很荣幸能够为这一重要突破提供优质产品,我们将继续致力于为科研工作者提供更优质的产品和服务。
本文内容基于《Advanced Science》(DOI: 10.1002/advs.202500844)原文献;文中涉及的原文献图片、数据等知识产权归原期刊及研究团队所有。若存在侵权情形,敬请及时联系我方删除,我方将积极配合处理。