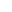- 手机:13761418683
电话:021-38015121
联系人:Absin
邮箱:zhouzz@univ-bio.com
网址:http://www.absin.cn/
地 址:上海市浦东新区新浩路58号18号楼

- 临床样本验证:通过 66 例 MP-LUAD 患者的组织芯片(MAPes 队列),确认 MYC 通路激活与 MP 表型的相关性,以及 MP-LUAD 特有的分子特征(如 EMT 标志物、抗剪切力标志物表达异常)。
- 体内外功能验证:分别在 LUAD 细胞系、小鼠移植瘤模型、斑马鱼异种移植模型中,验证 MYC 过表达需联合 M2 样巨噬细胞才能诱导 MP 表型(如极性改变、CTC 增多)。
- 机制深挖:通过 RNA-seq、ChIP-seq、CUT&Tag-seq 等技术,揭示 M2 样巨噬细胞分泌 TGFβ,诱导肿瘤细胞中 FOSL2 表达,进而重塑染色质可及性,促进 MYC 结合 MP 相关基因启动子的分子通路。
- 治疗靶点验证:使用 TGFβ 受体抑制剂 Galunisertib 阻断通路,有效逆转 MP 亚型的恶性表型,为临床治疗提供新方向。
解锁肺腺癌恶性进展新机制!揭示 MYC+M2 巨噬细胞调控新通路
2026-04-07
作为深耕生命科学研究工具领域的品牌,absin 始终聚焦科研前沿,助力科学家探索疾病发生发展的核心机制。近日,《Advanced Science》发表了重磅研究,揭示了微乳头亚型肺腺癌(MP-LUAD)的恶性进展调控新通路,而 absin 组织解离液为研究的顺利推进提供了重要支撑。
文献标题:Excessive MYC Orchestrates Macrophages induced Chromatin Remodeling to Sustain Micropapillary-Patterned Malignancy in Lung Adenocarcinoma
发表期刊:Advanced Science(IF 14.1) | DOI:https://doi.org/10.1002/advs.202403851
使用 Absin 产品:组织解离液(abs9482)

一、研究背景:MP-LUAD——极具侵袭性的“难治亚型”
肺腺癌(LUAD)是肺癌中最常见的亚型,其中微乳头亚型(MP)因高侵袭性、高转移率和差预后,成为临床治疗的难点。此前研究已知 MP-LUAD 具有锚定非依赖性生长、抗失巢凋亡等特性,但核心调控机制尚不明确。
团队发现 MP-LUAD 患者中 MYC 通路异常激活,但单独 MYC 过表达不足以诱导 MP 表型,推测肿瘤微环境中的免疫细胞可能发挥协同作用——这一关键洞察,成为本次研究的核心起点。
二、研究思路:层层递进,解锁“MYC+M2 巨噬细胞”协同调控网络
三、核心研究成果:四大突破,刷新对 MP-LUAD 的认知
1. 关键驱动通路:
MP-LUAD 的恶性进展依赖“MYC 过表达 + M2 样巨噬细胞浸润”的协同作用,单独任一因素均无法诱导完整 MP 表型。
2. 分子调控链:
M2 样巨噬细胞分泌的 TGFβ 激活肿瘤细胞中 FOSL2(先锋转录因子),FOSL2 打开 MP 相关基因的染色质结构,为 MYC 结合提供“靶点”,最终激活 EMT、抗失巢凋亡等恶性程序(对应原文图 6、7)。
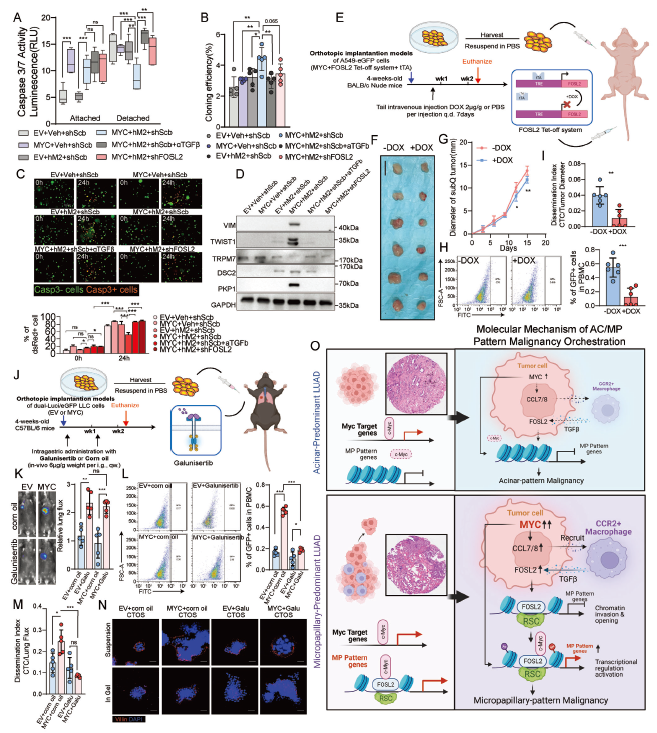
3. 细胞起源:
参与调控的 M2 样巨噬细胞主要来自骨髓造血干细胞,由 MYC 过表达的肿瘤细胞通过 CCL7/CCR2 通路招募(对应原文图 3)。
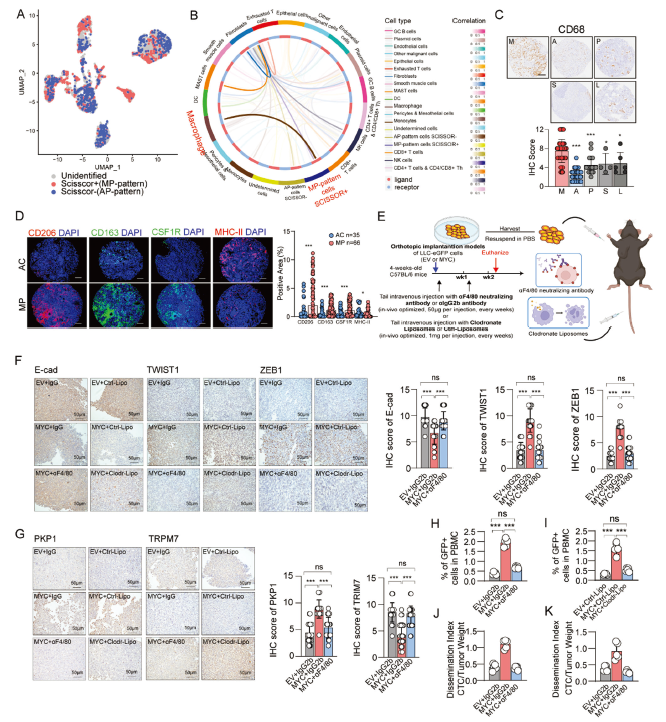
4. 治疗新靶点:
阻断 TGFβ-FOSL2 轴(如使用 Galunisertib)可显著降低 MP-LUAD 的转移能力,为临床精准治疗提供新策略(对应原文图 7J-N)。
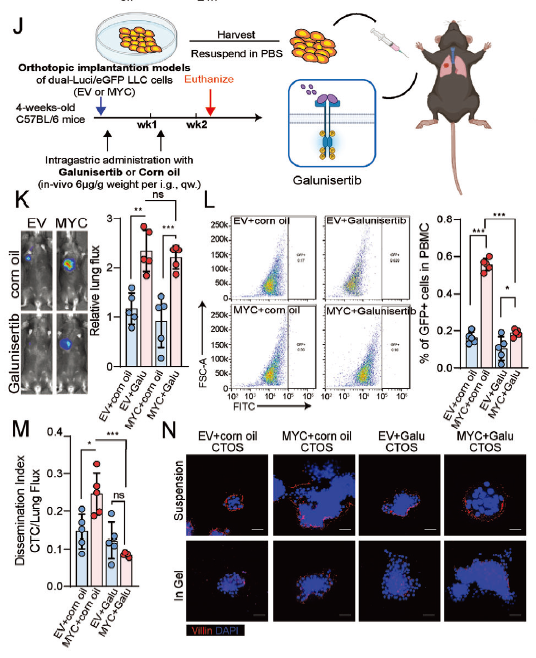
四、absin 产品助力:关键实验的“核心工具”
本次研究中,absin 的组织解离液(货号:abs9482)在肿瘤类器官(CTOS)制备中发挥了关键作用,直接支撑了 MP 表型相关的功能验证实验。
产品信息与应用场景
| 产品名称 | 货号 | 应用场景 |
|---|---|---|
| 组织解离液 | abs9482 | 从新鲜肿瘤组织中分离单细胞,用于制备肿瘤类器官(CTOS) |
产品在研究中的核心作用
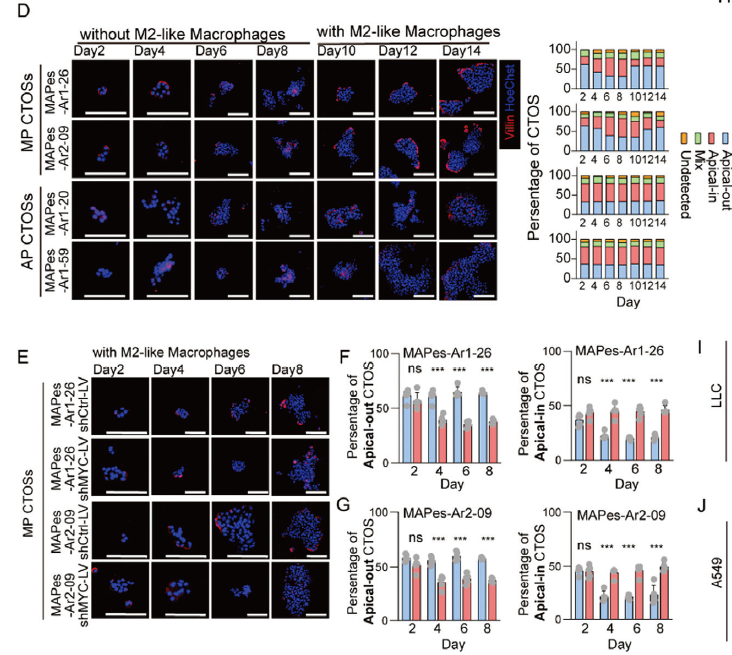
研究需通过患者来源的肿瘤类器官(CTOS)验证 MP 表型的极性特征——MP 来源的 CTOS 在 Matrigel 中培养时,会保持“顶向外”(apical-out)的独特极性,而这一表型是 MP-LUAD 锚定非依赖性生长的关键特征(对应原文图 1G、4D)。
absin 组织解离液凭借高效的组织消化能力,实现了从新鲜 MP-LUAD 组织中快速分离高活性单细胞,成功构建了可稳定传代的 CTOS 模型。后续通过免疫荧光染色(Villin 标记顶膜)验证极性变化,为“MYC+M2 巨噬细胞协同调控 MP 表型”提供了直接的功能学证据(对应原文图 4D-G)。
简言之,absin 组织解离液的可靠性能,确保了肿瘤类器官模型的成功构建,为体内外功能验证搭建了关键桥梁。
五、研究意义:从机制到转化,为 MP-LUAD 治疗开辟新路径
该研究首次揭示了 MP-LUAD 中“肿瘤细胞 - 免疫细胞 - 染色质重塑”的跨细胞调控网络,不仅加深了对肺癌亚型异质性的理解,更明确了 TGFβ-FOSL2 轴作为潜在治疗靶点的价值。
而 absin 作为科研工具提供者,始终以优质产品助力基础研究与临床转化的衔接——从组织样本处理到细胞功能验证,absin 产品正在为更多肿瘤机制研究、靶点发现提供可靠支持。
本文内容基于《Advanced Science》(DOI: 10.1002/advs.202403851)原文献;文中涉及的原文献图片、数据等知识产权归原期刊及研究团队所有。若存在侵权情形,敬请及时联系我方删除,我方将积极配合处理。