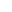- 手机:13761418683
电话:021-38015121
联系人:Absin
邮箱:zhouzz@univ-bio.com
网址:http://www.absin.cn/
地 址:上海市浦东新区新浩路58号18号楼

- FDFT1 敲低:抑制肝癌细胞增殖、迁移和转移,减少肿瘤负荷,改善小鼠肝功能;
- FDFT1 过表达:促进肝癌细胞增殖和转移,加速肿瘤进展。
- 关键数据:TCGA 和 ICGC 队列中,FDFT1 高表达患者的总生存期显著缩短(P<0.0001);90 例肝癌患者的 IHC 结果显示,FDFT1 高表达组肿瘤转移风险更高(P=0.024)。
- 关键证据:补充胆固醇或胆汁酸(CDCA)可逆转 FDFT1 敲低对肝癌细胞的抑制作用,恢复 AKT1 磷酸化水平。
- 捕获到与 AKT1 相互作用的 ALDOB 蛋白,证实两者直接结合(原文图 4E);
- 验证 HNF4A 与 ALDOB 启动子区域的特异性结合,为转录调控机制提供关键证据(原文图 5G)。
- 特异性强:试剂盒中的 Protein A/G Plus Agarose 可高效结合抗体 - 抗原复合物,减少非特异性结合;
- 操作便捷:优化的实验流程的,配套完整试剂,缩短实验周期;
- 结果可靠:低背景噪声确保蛋白相互作用检测的准确性,为机制验证提供坚实数据支撑。
胆固醇代谢紊乱促癌:顶刊证实 FDFT1 为关键靶点并揭示 HNF4A/ALDOB/AKT1 轴调控机制
2026-04-13
文献标题:Targeting FDFT1 Reduces Cholesterol and Bile Acid Production and Delays Hepatocellular Carcinoma Progression Through the HNF4A/ALDOB/AKT1 Axis
发表期刊:Advanced Science(IF 14.1) | DOI:https://doi.org/10.1002/advs.202411719
使用 Absin 产品:免疫(共)沉淀(IP/CoIP)试剂盒(abs955)


一、研究背景:肝癌治疗的痛点与新方向
肝癌是全球癌症相关死亡的第三大原因,其中肝细胞癌(HCC)占比约 90%。尽管靶向治疗取得了一定进展,但不可切除肝癌患者的中位总生存期仍不足 2 年。胆固醇代谢异常被证实是肝癌发生发展的重要驱动因素,而传统降脂药物他汀类在肝癌治疗中的应用存在争议(疗效不佳且易引发不良反应),因此亟需寻找新的胆固醇代谢相关靶点。
法尼基焦磷酸法尼基转移酶 1(FDFT1)是胆固醇生物合成通路中的关键酶,其在不同肿瘤中的作用存在差异,但在肝癌中的功能尚不明确。基于此,研究团队围绕 FDFT1 展开系统研究,旨在验证其作为肝癌治疗靶点的潜力及相关分子机制。
二、研究思路:层层递进,解锁 FDFT1 的肝癌调控网络
1. 靶点筛选:从海量基因中锁定核心分子
研究团队首先通过整合 TCGA、ICGC、GEO 等公共数据库的肝癌样本数据,筛选出胆固醇生物合成通路中的 23 个关键基因。结合差异表达基因(DEGs)分析和单变量 Cox 分析,最终发现 FDFT1 在肝癌组织中高表达,且与患者不良预后密切相关,成为后续研究的核心靶点。
2. 功能验证:体内外实验确认 FDFT1 的促癌作用
为明确 FDFT1 对肝癌的影响,研究团队通过细胞实验(CCK8、克隆形成、EdU 标记、迁移侵袭实验)和动物模型(皮下移植瘤、肺转移模型、DEN/CCL?诱导肝癌模型),从正反两方面验证:
3. 机制深挖:解析 FDFT1 调控肝癌的分子通路
通过 RNA-seq、Co-IP、ChIP-qPCR 等技术,研究团队逐步揭示核心机制:FDFT1 敲低→胆固醇和胆汁酸水平下降→增强 HNF4A 转录活性→HNF4A 结合 ALDOB 启动子并促进其转录→ALDOB 与 AKT1 结合抑制其磷酸化→最终抑制肝癌进展(HNF4A/ALDOB/AKT1 轴)。
4. 联合治疗探索:提升临床转化潜力
鉴于 AKT 抑制剂(AZD5363)在肝癌中的应用现状,研究团队进一步验证 FDFT1 敲低与 AZD5363 联合治疗的效果,发现该联合方案能显著增强抗肿瘤活性,为临床治疗提供新策略。
三、核心研究成果:四大关键发现,点亮肝癌治疗新希望
1. FDFT1 是肝癌不良预后标志物
临床样本和公共数据库分析证实,FDFT1 在肝癌组织中高表达,与肿瘤大小、远处转移、BCLC 分期正相关,是肝癌患者预后不佳的独立危险因素(原文图 1)。
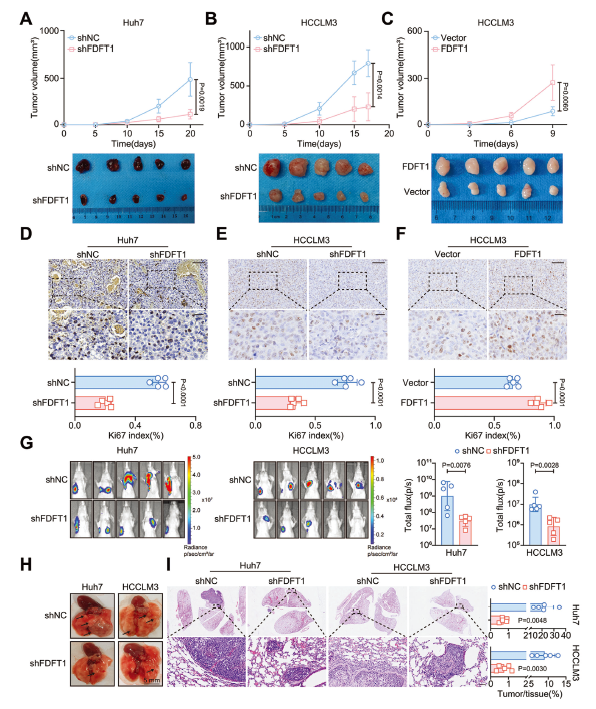
2. FDFT1 通过代谢重编程促进肝癌
FDFT1 作为胆固醇合成关键酶,其表达水平直接影响细胞内胆固醇和胆汁酸含量,而这两种物质可通过抑制 HNF4A 转录活性,间接促进 AKT1 磷酸化,推动肝癌进展(原文图 6)。
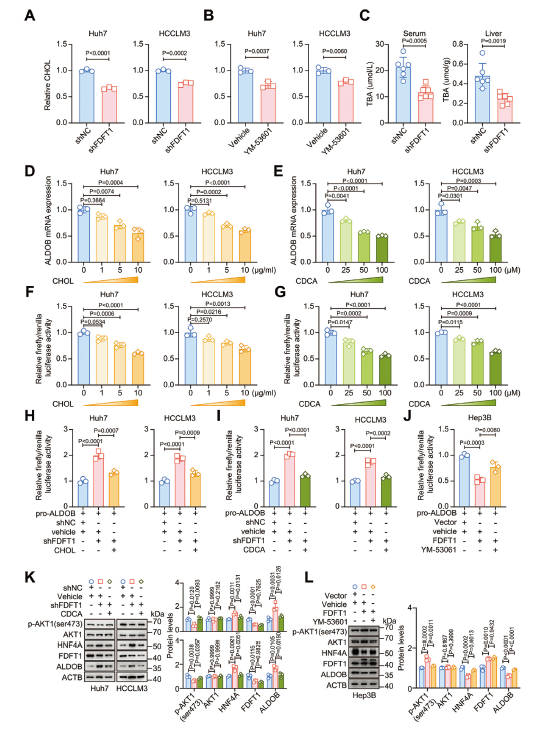
3. HNF4A/ALDOB/AKT1 轴是核心调控通路
这是研究首次揭示该轴在胆固醇代谢与肝癌进展中的桥梁作用,其中 ALDOB 作为关键节点,连接代谢重编程与信号通路调控(原文图 4、图 5)。
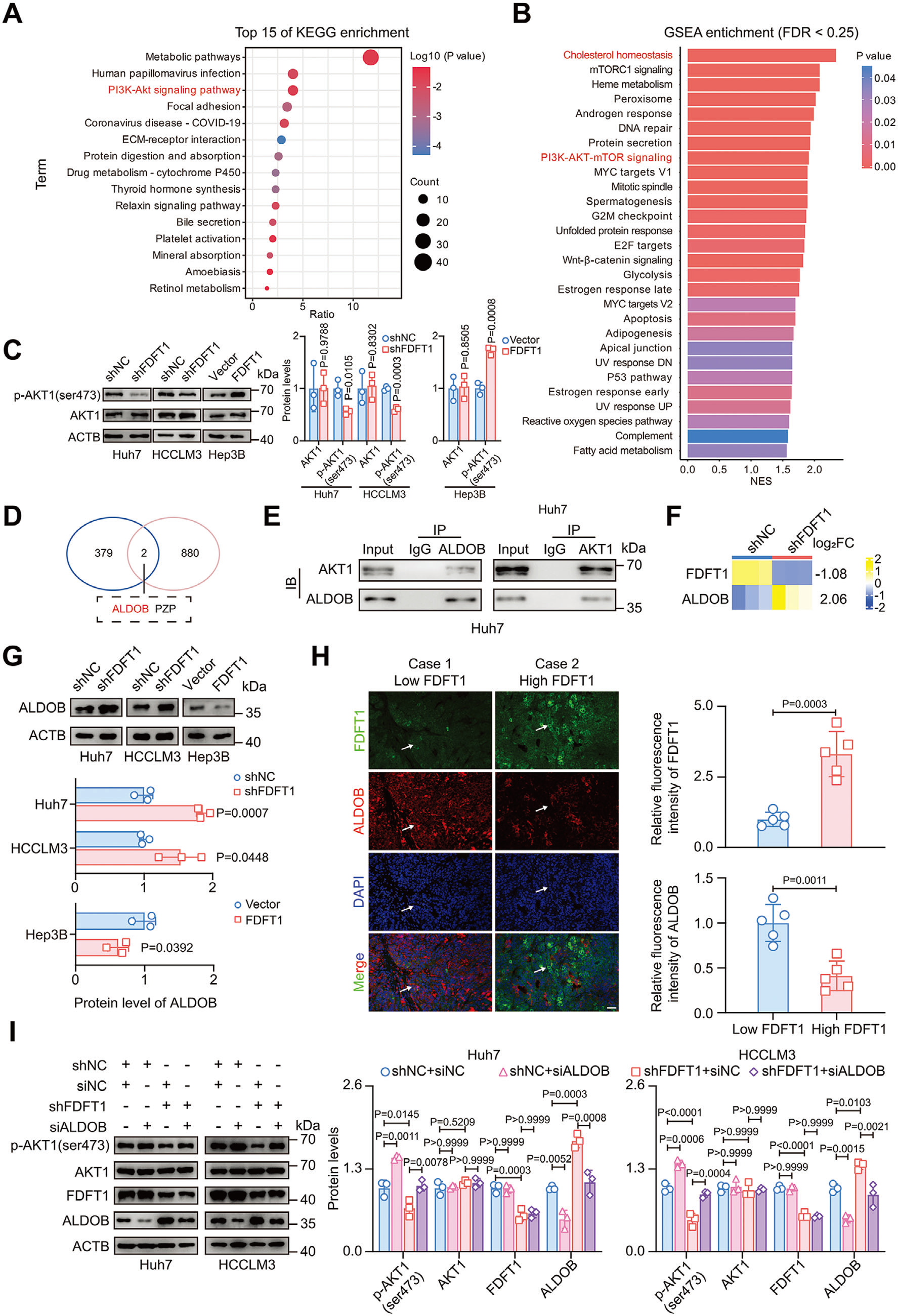
FDFT1 通过 ALDOB 抑制 AKT1 磷酸化(FDFT1 knockdown impairs AKT1 phosphorylation via ALDOB to inhibit HCC)

HNF4A 直接调控 ALDOB 转录(FDFT1 knockdown activates HNF4A to promote ALDOB expression)
4. FDFT1 靶向联合 AKT 抑制剂疗效显著
体内外实验证实,FDFT1 敲低可增强肝癌细胞对 AZD5363 的敏感性,联合治疗组的肿瘤体积和重量显著小于单药组(原文图 7),为临床联合用药提供了新方案。
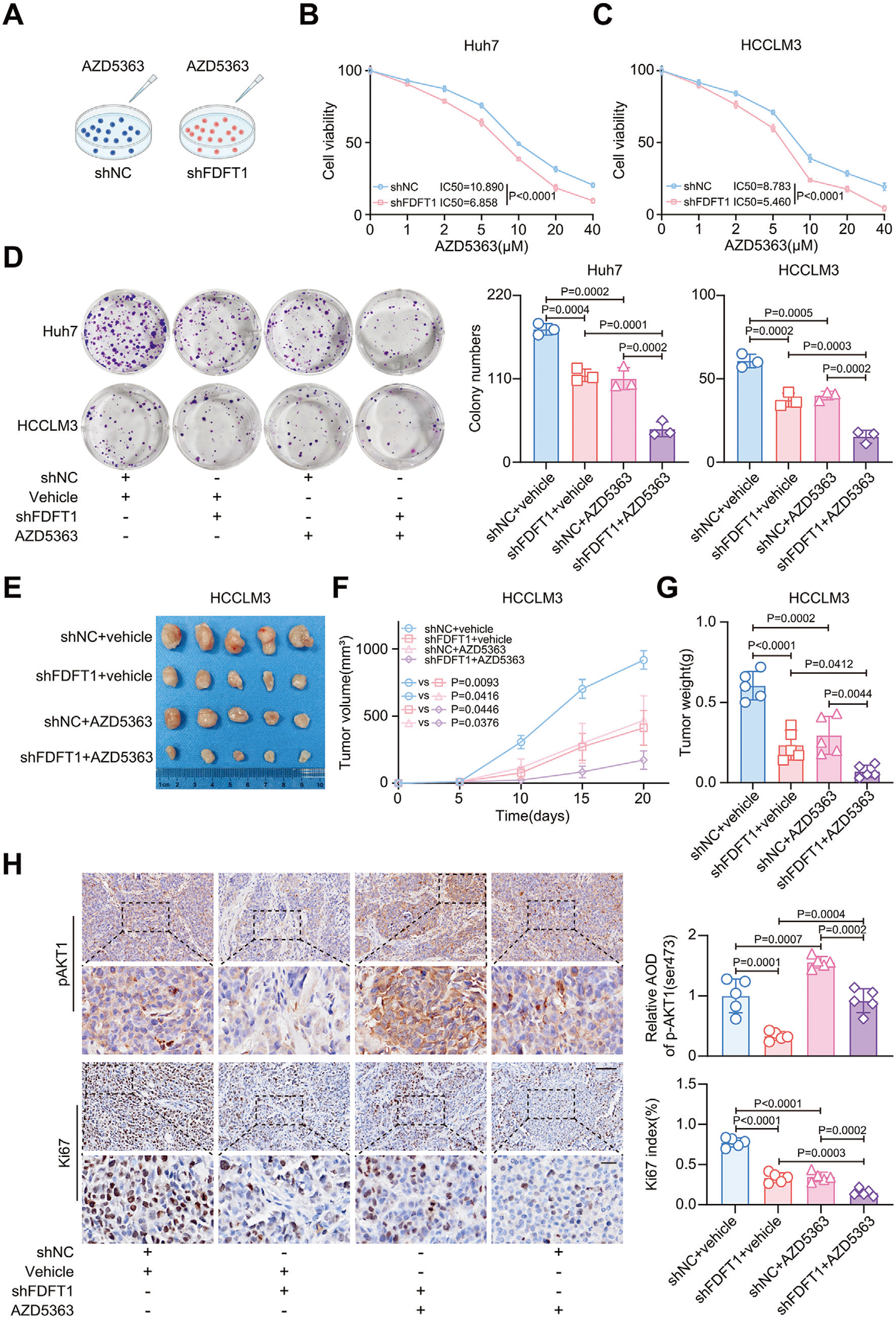
FDFT1 靶向与 AZD5363 联合治疗效果(Targeting FDFT1 boosts sensitivity to capivasertib (AZD5363) in HCC)
四、absin 产品赋能:关键实验的可靠工具支持
在这项机制复杂、实验设计严谨的研究中,absin 的 免疫共沉淀(Co-IP)试剂盒(产品编号:abs955) 发挥了不可或缺的作用。
产品应用场景:
研究团队为明确 AKT1 的相互作用蛋白,以及 HNF4A 与 ALDOB 启动子的结合关系,需通过 Co-IP 实验捕获蛋白复合物。absin 的 Co-IP 试剂盒凭借高效的蛋白结合效率和低背景干扰,成功助力研究团队:
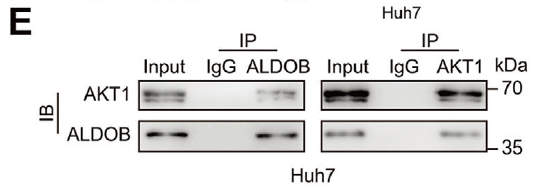
|
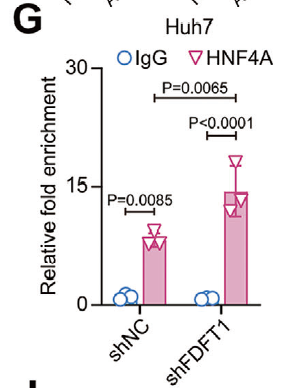
|
产品核心优势:
五、总结与展望:从基础研究到临床转化的新可能
该研究不仅首次系统阐明了 FDFT1 在肝癌中的促癌作用及分子机制,还为肝癌治疗提供了新的靶点和联合治疗策略。FDFT1 作为他汀类药物的潜在替代靶点,其靶向抑制剂与 AKT 抑制剂的联合方案,有望解决传统治疗的局限性,为肝癌患者带来新的生存希望。
absin 始终致力于为科研工作者提供高品质的实验工具,从 Co-IP 试剂盒到各类抗体、检测试剂,我们的产品已广泛应用于肿瘤代谢、信号通路、靶向治疗等多个研究领域。未来,absin 将持续聚焦生命科学前沿,不断优化产品性能,助力更多创新性研究突破,为疾病治疗的临床转化贡献力量!
本文内容基于《Advanced Science》(DOI: 10.1002/advs.202411719)原文献;文中涉及的原文献图片、数据等知识产权归原期刊及研究团队所有。若存在侵权情形,敬请及时联系我方删除,我方将积极配合处理。