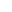- 手机:13761418683
电话:021-38015121
联系人:Absin
邮箱:zhouzz@univ-bio.com
网址:http://www.absin.cn/
地 址:上海市浦东新区新浩路58号18号楼

-
疫苗构建:以毕赤酵母为载体,分别构建膜锚定型(YVm)和分泌型(YVs) RBD 酵母疫苗。YVm 通过 GPI 锚定将 RBD 展示于酵母表面,YVs 则通过信号肽实现 RBD 分泌。
- 体外特性验证:检测疫苗的 RBD 表达、糖基化修饰、胃肠道稳定性及树突状细胞(DC)激活能力。
- 体内分布追踪:通过 DiD 标记追踪疫苗在小鼠肠道、派氏结(PP)及肠系膜淋巴结(MLN)的定植与细胞摄取情况。
- 免疫效应评估:检测疫苗诱导的 RBD 特异性 IgA/IgG 抗体水平及假病毒中和能力。
- 机制解析:通过单细胞测序和转录组分析,阐明疫苗激活 DC-Tfh-B 细胞互作的免疫机制。
- 竞品对比:将酵母疫苗与细菌锚定疫苗(BVm)、细胞膜仿生纳米疫苗(CNV)对比,验证其免疫优势。
-
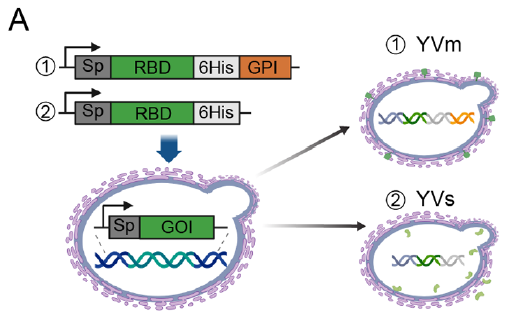
经免疫印迹验证,YVm 的 RBD 实现膜锚定表达且存在糖基化修饰(分子量约 60kDa,去糖基化后为 35kDa),而 YVs 为分泌型表达(对应原文图 2B、2C);
-
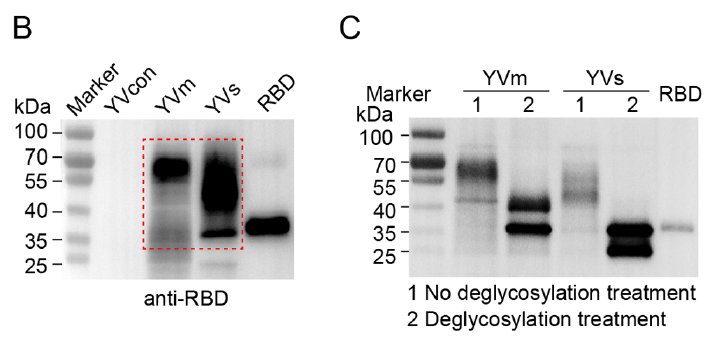
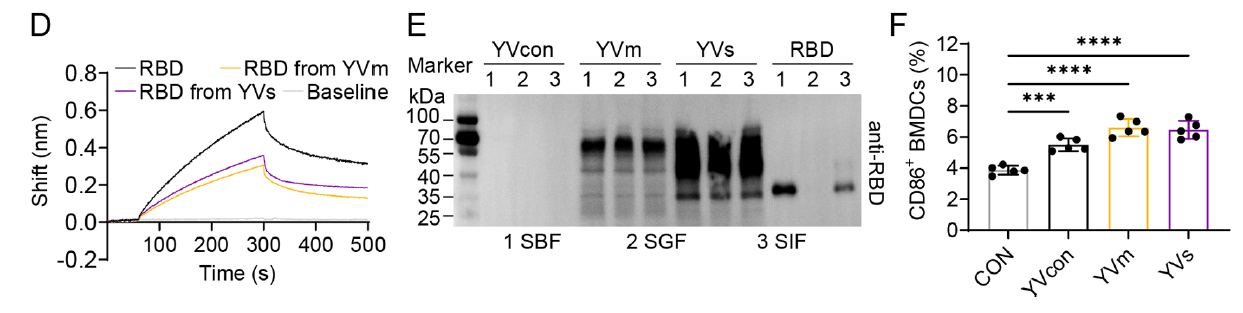
YVm 的 RBD 可与 ACE2 高效结合,且在模拟胃肠液中稳定性优异,能有效激活骨髓来源树突状细胞(BMDC)成熟(对应原文图 2D-2F);
-
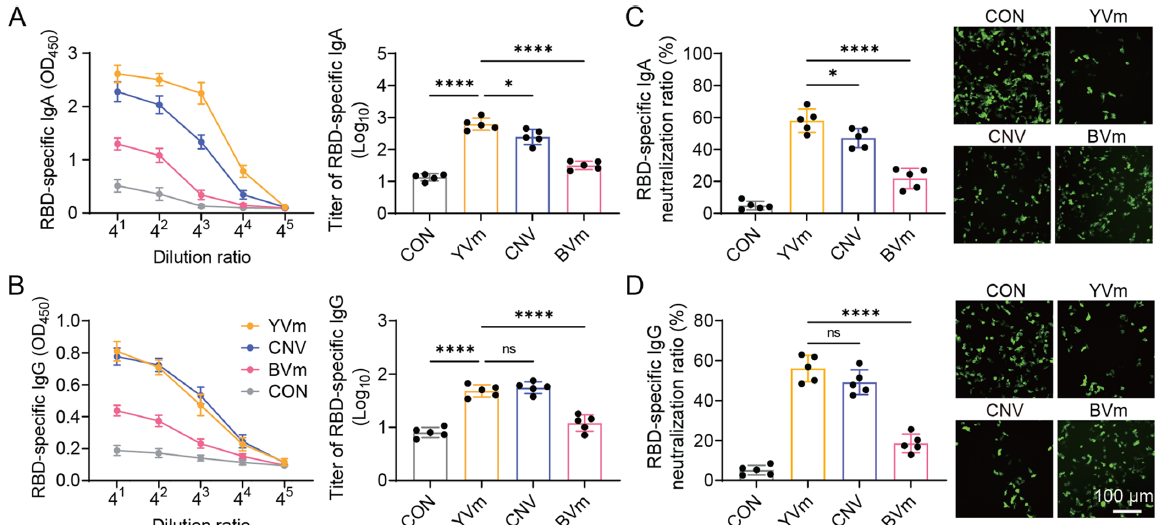
免疫小鼠肠道黏膜的 RBD 特异性 sIgA 滴度达 103 量级,血清 IgG 水平较 YVs 组高 30%-40%(对应原文图 5A、5B);
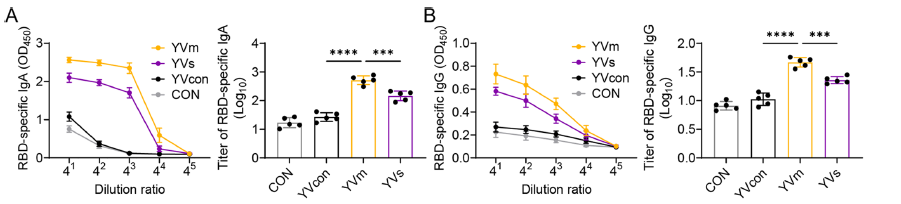
-
肠道灌洗液中的 IgA 对 SARS-CoV-2 假病毒的中和率超 60%,血清 IgG 也展现出强中和活性,显著优于 YVs 组(对应原文图 5D、5E);
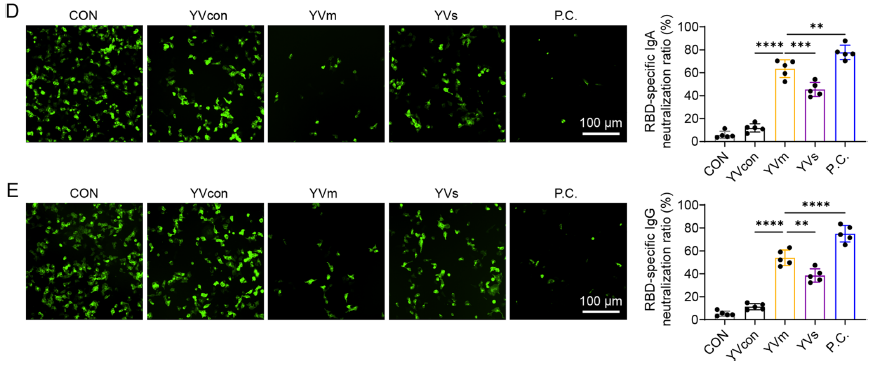
-
作为免疫印迹阳性对照:在验证 YVm 和 YVs 的 RBD 表达实验中,研究团队使用 50ng Absin RBD 蛋白作为阳性对照,精准判定酵母疫苗中 RBD 的表达效率及分子量(对应原文图 2B)。
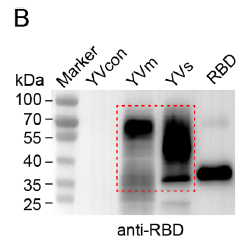
- 校准抗原活性检测体系:在验证 RBD 与 ACE2 的结合活性、模拟胃肠液中 RBD 稳定性等实验中,Absin RBD 蛋白作为标准品,确保了实验数据的准确性和可比性。
比细菌 / 纳米疫苗更优!这款锚定酵母疫苗解决黏膜疫苗 IgA 分泌不足痛点
2026-03-25
在全球感染性疾病防控领域,黏膜免疫因其能在病原体入侵的第一道防线建立保护屏障,成为疫苗研发的核心方向之一。近期,一项发表于《ACS Nano》的研究(doi:10.1021/acsnano.4c14690)成功开发出抗原锚定型酵母口服疫苗,为黏膜疫苗的临床转化提供了全新方案。值得关注的是,Absin 的重组 SARS-CoV-2 RBD 蛋白在该研究中作为关键实验材料,为疫苗的免疫原性验证等核心环节提供了重要支持。
文献标题:Orally Antigen-Engineered Yeast Vaccine Elicits Robust Intestinal Mucosal Immunity
发表期刊:ACS Nano(IF 16)
DOI:https://doi.org/10.1021/acsnano.4c14690
使用Absin试剂:Recombinant SARS-CoV-2 Spike RBD Protein(abs05113)

一、研究背景:黏膜疫苗研发的痛点与突破方向
黏膜是人体抵御病原体入侵的第一道防线,肠道黏膜更是与外界微生物接触的重要界面。但传统黏膜疫苗面临抗原展示效率低、佐剂安全性不足两大难题,难以同时激活先天和适应性黏膜免疫。
基于此,研究团队将目光投向酵母表达系统:一方面,酵母自身的 β- 葡聚糖可作为天然安全佐剂;另一方面,真核酵母能实现抗原的糖基化修饰,更接近天然病毒抗原的结构。团队创新性地设计了 “抗原锚定” 和 “抗原分泌” 两种酵母疫苗模式,以 SARS-CoV-2 的 RBD 为模型抗原,探索最优的黏膜免疫激活策略。
二、核心研究思路:从疫苗构建到免疫机制解析
研究整体遵循 “疫苗设计 - 体外验证 - 体内分布 - 免疫效应 - 机制解析 - 竞品对比” 的完整逻辑链,层层递进验证抗原锚定型酵母疫苗的优势:
三、关键研究成果:抗原锚定型酵母疫苗实现强效黏膜免疫
1. YVm 的体外特性更优
2. YVm 可高效靶向肠道免疫位点
口服后 YVm 可在小鼠小肠定植 6-12h,6h 时在派氏结、12h 时在肠系膜淋巴结达到荧光信号峰值,且能被 M 细胞、B 细胞及 DC 高效摄取(对应原文图 3A-I)。
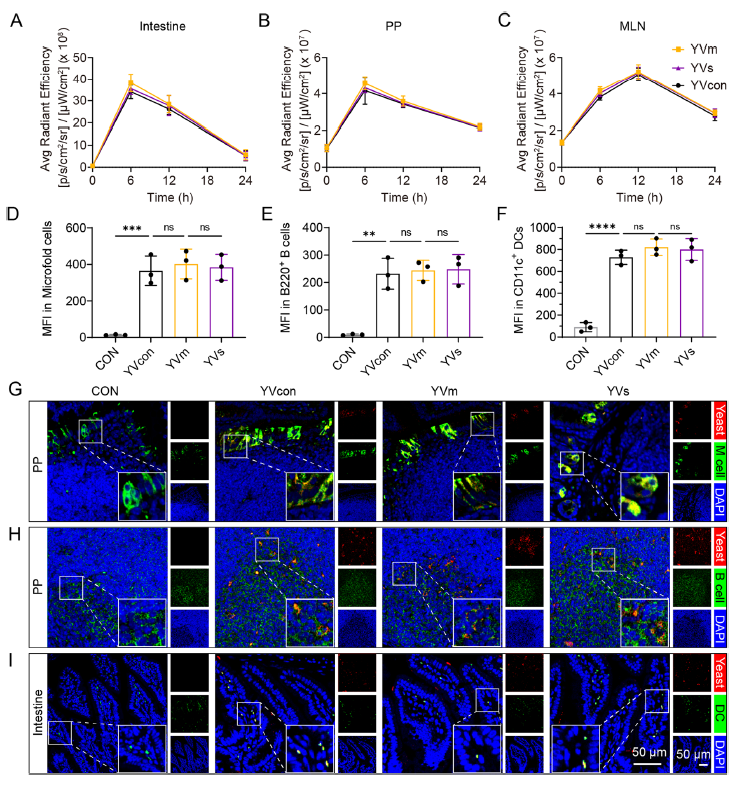
3. YVm 激活强效黏膜及全身免疫
4. YVm 的免疫机制更具优势
转录组及单细胞测序显示,YVm 可显著促进派氏结和肠系膜淋巴结中 DC 成熟、Tfh 细胞分化及生发中心 B 细胞激活,上调 CCR7、CXCR5 等趋化因子表达,强化 T-B 细胞互作(对应原文图 4、图 6)。
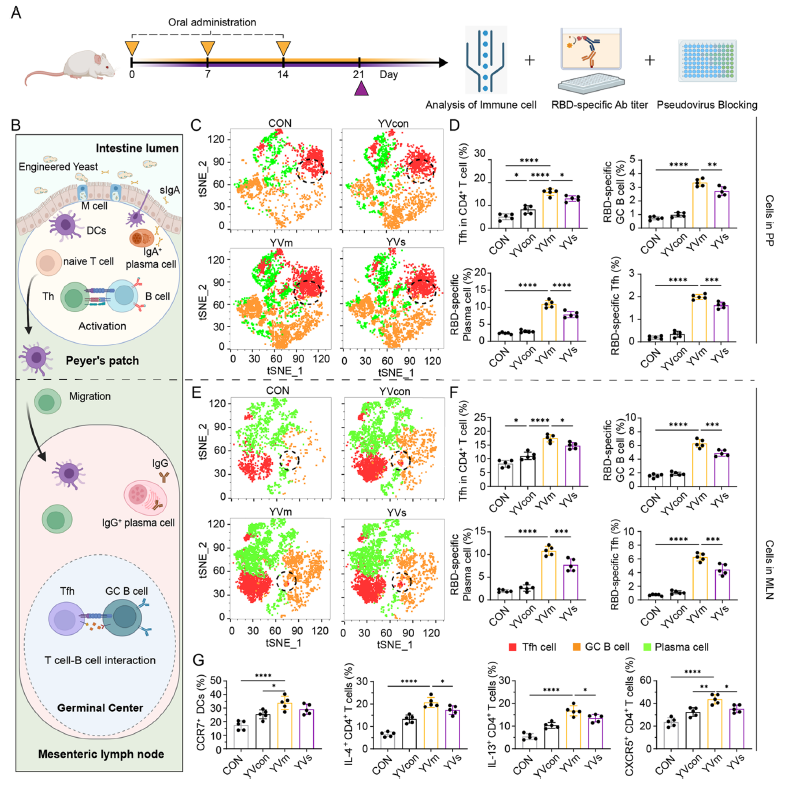
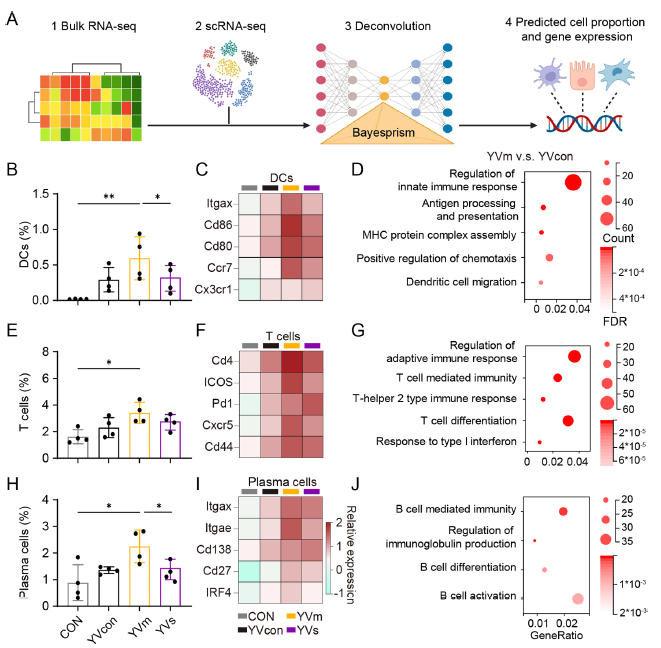
5. YVm 优于其他细胞源疫苗
对比 BVm 和 CNV,YVm 诱导的 RBD 特异性 IgA/IgG 水平及假病毒中和能力均居首位,且无明显毒性(对应原文图 7)。
四、Absin 产品的关键支撑作用
在整个研究中,Absin 重组 SARS-CoV-2 RBD 蛋白(货号 abs05113) 承担了核心的实验参照与验证功能,具体作用如下:
Absin 重组 RBD 蛋白凭借高纯度、高活性的产品特性,为研究中疫苗抗原的表达验证和活性评估提供了可靠的原料保障,助力科研团队高效完成核心实验环节。
五、研究意义与应用前景
该研究首次阐明了抗原展示模式对酵母黏膜疫苗免疫效果的影响,证实膜锚定型酵母疫苗可通过整合 “天然佐剂 + 糖基化抗原” 实现强效黏膜免疫。而 Absin 产品在研究中的关键应用,也体现了高品质生物试剂对前沿疫苗研发的重要支撑价值。
本文内容基于《ACS Nano》(DOI: 10.1021/acsnano.4c14690)原文献;文中涉及的原文献图片、数据等知识产权归原期刊及研究团队所有。若存在侵权情形,敬请及时联系我方删除,我方将积极配合处理。