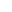- 手机:13761418683
电话:021-38015121
联系人:Absin
邮箱:zhouzz@univ-bio.com
网址:http://www.absin.cn/
地 址:上海市浦东新区新浩路58号18号楼

从机制到转化:仿生p62纳米平台NanoTAC??? 打通细胞器靶向治疗的最后一公里
2026-03-25
在肿瘤治疗领域,细胞器靶向干预因其精准性和高效性成为研究热点。近日,一项发表于《ACS Nano》的研究(doi:10.1021/acsnano.5c10801)创新性地开发了模拟 p62 聚集体的模块化纳米组装体 NanoTAC???,实现了对线粒体、内质网、高尔基体等细胞器的精准捕获与降解,为乳腺癌治疗提供了全新方案。作为实验过程中的关键试剂供应商,Absin 基质胶为该研究的顺利推进提供了重要支撑。
文献标题:Modular Nanoassemblies Mimicking p62 Aggregates for Targeted Organelle Sequestration and Degradation against Breast Cancer
发表期刊:ACS Nano(IF 16)
DOI:https://doi.org/10.1021/acsnano.5c10801
使用Absin试剂:基质胶(标准型,含酚红)(abs9490)

一、研究思路:仿生p62,突破传统降解技术瓶颈
传统靶向蛋白降解工具(如 PROTACs)依赖泛素 - 蛋白酶体系统,难以实现对线粒体、内质网等大型细胞器的降解。而细胞内的选择性自噬依赖 p62 等受体的多价识别形成聚集体,通过液 - 液相分离包裹受损细胞器并完成清除。
基于此,研究团队提出 仿生 p62 聚集体的纳米靶向嵌合体(NanoTAC???) 设计思路:以 PLGA 为核心,整合溶酶体逃逸模块(GALA 肽)、细胞器靶向模块、LC3B 结合模块,通过多价相互作用实现细胞器的聚类、捕获,并招募自噬体完成降解。该平台可灵活替换靶向配体,实现对不同细胞器的选择性降解,且无传统降解剂的 “钩效应”。
二、核心研究成果:多维度验证NanoTAC???的治疗潜力
1. 线粒体靶向降解(NanoTAC????)实现代谢重编程
研究团队首先构建线粒体靶向的 NanoTAC????,通过 TSPO 配体靶向肿瘤细胞线粒体,同时借助 LC3B 结合模块招募自噬体。实验证实,NanoTAC????可高效诱导线粒体聚集并降解,破坏氧化磷酸化(OXPHOS)通路;而肿瘤细胞会启动代偿性糖酵解,此时联合 GLUT1 抑制剂 BAY-876 可实现 “OXPHOS + 糖酵解” 双代谢抑制。
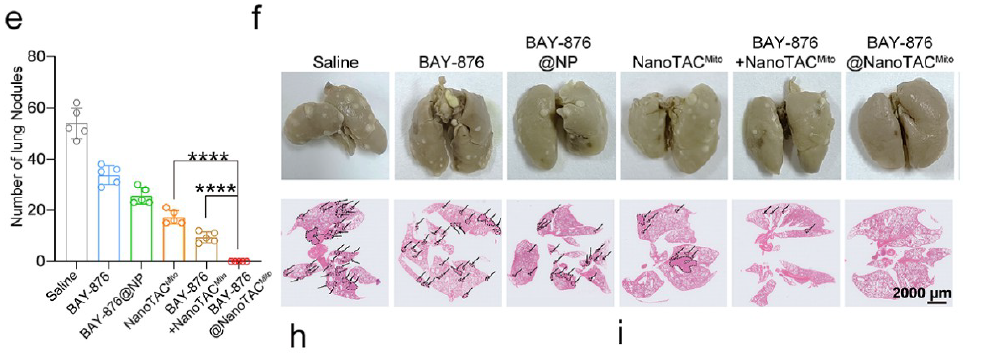
体内实验显示,BAY-876@NanoTAC????可显著抑制 4T1 乳腺癌模型的肿瘤生长、复发及肺转移,且无明显全身毒性(对应原文Figure 6)。
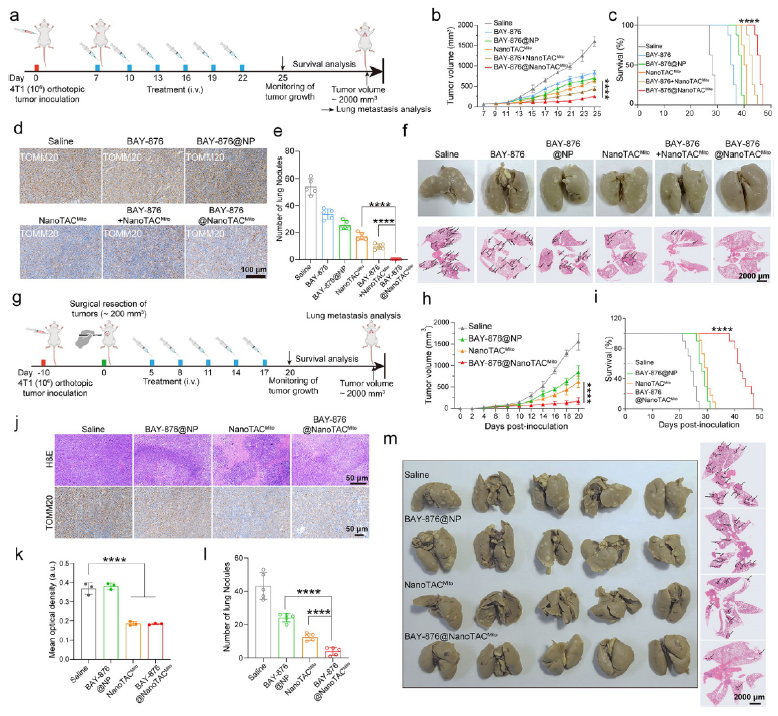
2. 拓展至内质网与高尔基体的广谱降解
通过替换靶向配体,研究团队成功开发 NanoTAC??(靶向内质网 SUR1)和 NanoTAC?????(靶向高尔基体 COX-2),实现了对这两类复杂网状细胞器的有效降解。实验表明,NanoTAC??和 NanoTAC?????可诱导细胞器聚集、溶酶体共定位,进而触发肿瘤细胞毒性(对应原文Figure 7)。
3. 技术优势显著
相较于传统小分子降解剂,NanoTAC???具备三大核心优势:①无钩效应,高浓度下仍保持降解活性;②模块化设计,可快速适配不同细胞器靶点;③载体功能,可包载化疗 / 靶向药物实现联合治疗。
三、Absin 产品:助力实验顺利推进的关键支撑
| Absin 产品 | 对应实验环节 | 文中作用 |
|---|---|---|
| Matrigel(abs9490) | 体外3D侵袭实验(Transwell实验) | 铺制Transwell小室基质胶,构建肿瘤细胞体外侵袭模拟微环境,评估NanoTAC???对4T1细胞侵袭能力的抑制效果 |
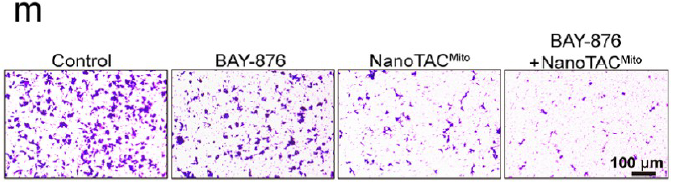
在肿瘤细胞侵袭能力验证实验中,研究团队将 4T1 细胞接种于铺有 Absin Matrigel 的 Transwell 上室,下室加入含 10% FBS 的培养基,同时给予不同 NanoTAC???处理。Matrigel 作为基底膜基质,可模拟体内肿瘤细胞侵袭过程中的细胞外基质(ECM)屏障,精准反映药物对肿瘤细胞穿透 ECM 能力的影响。
实验结果显示,NanoTAC????联合 BAY-876 可显著降低穿膜细胞数量,证实其对肿瘤侵袭的抑制作用(相关数据支撑原文Figure 5m、Figure 6e-f等肿瘤转移相关结论)。Absin Matrigel 的高生物活性和均一性,为实验结果的可靠性提供了重要保障。
四、研究意义与应用前景
该研究首次实现了基于纳米载体的多细胞器广谱靶向降解,不仅为乳腺癌治疗提供了 “代谢干预 + 靶向降解” 的双效策略,也为其他难治性肿瘤的细胞器靶向治疗开辟了新方向。而 Absin 高品质生物试剂的助力,也再次印证了实验工具对前沿科研的重要支撑作用。
未来,随着 NanoTAC???平台的进一步优化(如响应性释药、多靶点协同),结合 Absin 丰富的科研试剂产品线,有望加速该技术向临床转化,为肿瘤精准治疗注入新动力。
本文内容基于《ACS Nano》(DOI: 10.1021/acsnano.5c10801)原文献;文中涉及的原文献图片、数据等知识产权归原期刊及研究团队所有。若存在侵权情形,敬请及时联系我方删除,我方将积极配合处理。