- 手机:13761418683
电话:021-38015121
联系人:Absin
邮箱:zhouzz@univ-bio.com
网址:http://www.absin.cn/
地 址:上海市浦东新区新浩路58号18号楼

- IRF8 过表达(Irf8-OE)小鼠:AAA 扩张更严重,主动脉弹性纤维断裂、胶原沉积增加,炎症细胞浸润显著(原文图 2A-E)。
- IRF8 树突状细胞特异性敲除(Irf8ΔDC)小鼠:AAA 扩张被显著抑制,主动脉结构损伤减轻,炎症反应减弱(原文图 2F-J)。
- cDC1 可激活 CD8+T 细胞:Irf8-OE 小鼠中,CD8+T 细胞成熟标志物(CD69)及细胞因子(TNF-α、IFN-γ)表达显著升高(原文图 4A-F);反之,Irf8ΔDC 小鼠中 CD8+T 细胞活化受抑(原文图 4G-H)。
- 阻断该轴可缓解 AAA:抑制 cDC1 与 CD8+T 细胞的相互作用(Clec9a-/- 小鼠或 CLEC9A 中和抗体),能有效减轻 AAA 扩张(原文图 4I-L)。
- 最终效应:活化的 CD8+T 细胞通过诱导血管平滑肌细胞凋亡,破坏主动脉壁结构(原文图 5A-F)。
- 实现多标志物同步检测:在同一张组织切片上同时标记 IRF8(绿色)和穿孔素(黄色),清晰呈现两者在 AAA 组织中的共定位关系(原文图 7A)。
- 信号放大与特异性保障:HRP 偶联二抗高效结合一抗,TSA 技术显著增强荧光信号,确保低表达标志物的精准检出,为 “人类 AAA 组织中 IRF8 高表达且与细胞毒性增强相关” 的结论提供了直接可视化证据(原文图 7C)。
- 数据可靠性支撑:该实验结果与小鼠模型数据相互印证,证实 IRF8-cDC1-CD8+T 细胞轴在人类 AAA 中同样发挥作用,为研究的临床转化价值奠定基础。
突破 AAA 研究瓶颈!解析 IRF8?cDC1?CD8+T 细胞轴致病机制
2026-04-21
腹部主动脉瘤(AAA)作为全球高发的致命性血管疾病,其发病机制复杂且缺乏有效药物治疗。近期,发表于《Advanced Science》的一项重磅研究,首次明确了 IRF8(干扰素调节因子 8)通过驱动 cDC1(1 型常规树突状细胞)分化和 CD8+T 细胞活化,加剧主动脉壁损伤的关键作用,为 AAA 的靶向治疗提供了全新方向。 Absin mIHC 试剂盒助力该研究的关键实验环节,见证了这一重要科研突破。
文献标题:IRF8 Drives Conventional Type 1 Dendritic Cell Differentiation and CD8+ T Cell Activation to Aggravate Abdominal Aortic Aneurysm Development
发表期刊:Advanced Science(IF 14.1) | DOI:https://doi.org/10.1002/advs.202416238
使用 Absin 产品:七色多重荧光免疫组化染色试剂盒(鼠兔通用二抗)(abs50015)

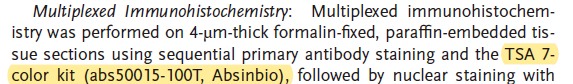
一、研究思路:聚焦免疫细胞轴,破解 AAA 致病谜题
1. 提出科学问题:已知树突状细胞(DCs)在 AAA 发展中起关键作用,但具体亚型及调控机制尚不明确,IRF8 作为 cDC1 发育的核心调控因子,是否参与 AAA 病理进程?
2. 构建研究框架:从 “临床样本验证 - 动物模型干预 - 细胞分子机制 - 人体数据佐证” 层层递进,全面解析 IRF8 的作用及下游通路。
3. 核心验证逻辑:通过 IRF8 过表达、敲除小鼠模型,结合 cDC1 缺陷小鼠(Batf3-/-)和细胞实验,明确 IRF8-cDC1-CD8+T 细胞轴与 AAA 的关联。
二、研究成果:四大关键发现,重塑 AAA 免疫治疗认知
1. IRF8 在 AAA 中异常高表达
人类 AAA 组织和小鼠模型中,IRF8 在 HLA-DR+ 树突状细胞中显著富集,且表达水平与 AAA 严重程度正相关(原文图 1D-F)。这一发现首次证实 IRF8 与 AAA 发病的密切关联,为后续机制研究奠定基础。
2. IRF8 调控 AAA 发展的双向作用
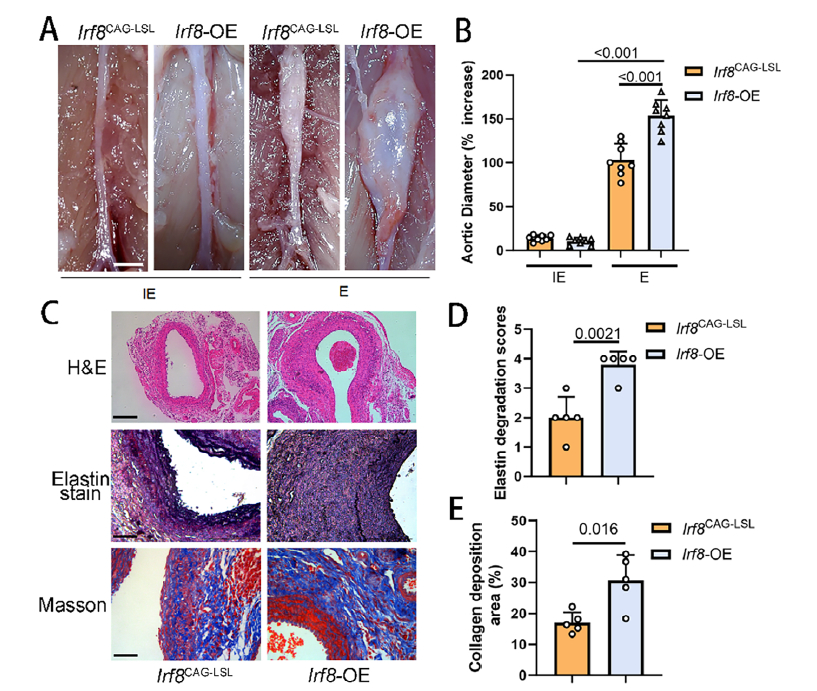
IRF8 过表达小鼠 AAA 表型分析(原文图 2A-E)
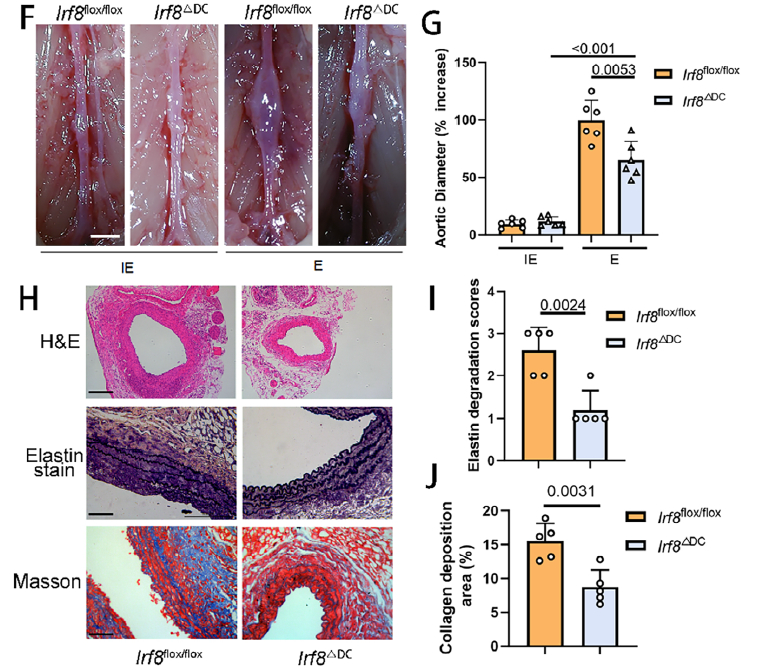
IRF8 敲除小鼠 AAA 表型分析(原文图 2F-J)
3. cDC1 是 IRF8 的关键下游效应细胞
单细胞测序和流式细胞术证实,cDC1 是 AAA 微环境中 IRF8 的主要表达细胞(原文图 3A-D)。而 cDC1 缺陷的 Batf3-/- 小鼠,其 AAA 表型与 Irf8ΔDC 小鼠高度一致,证明 IRF8 通过调控 cDC1 发挥作用(原文图 3E-F)。
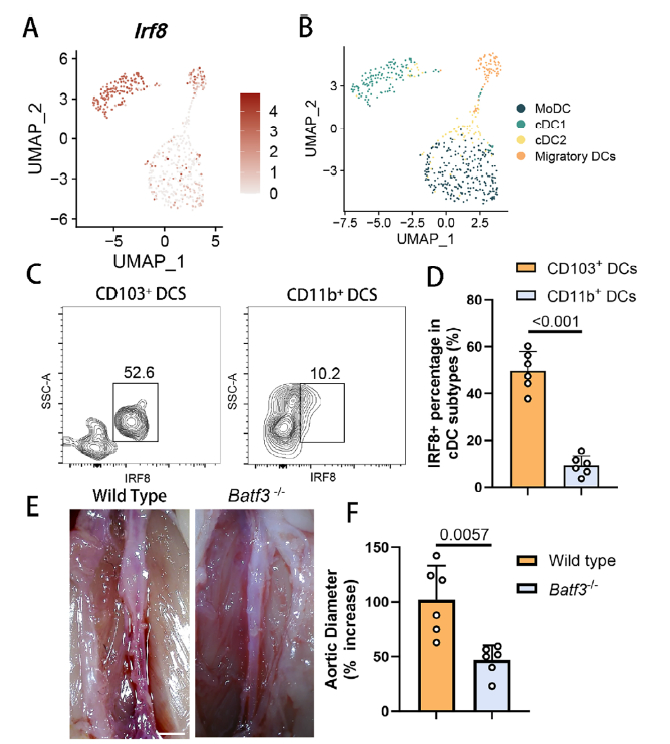
cDC1 作为 IRF8 下游效应细胞的验证(原文图 3A-F)
4. IRF8-cDC1-CD8+T 细胞轴介导主动脉损伤
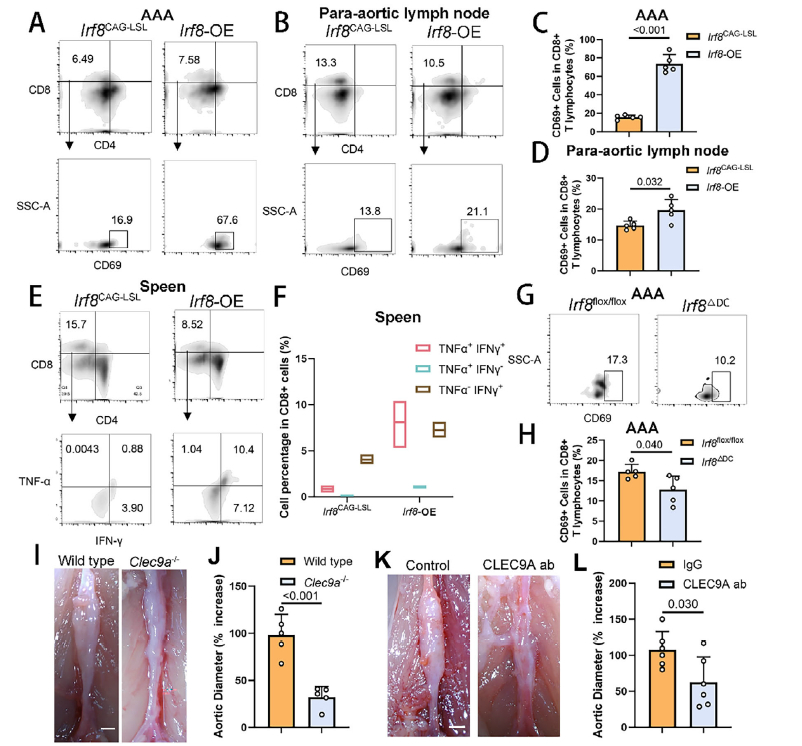
IRF8-cDC1-CD8+T 细胞轴调控 AAA 发展(原文图 4A-L)
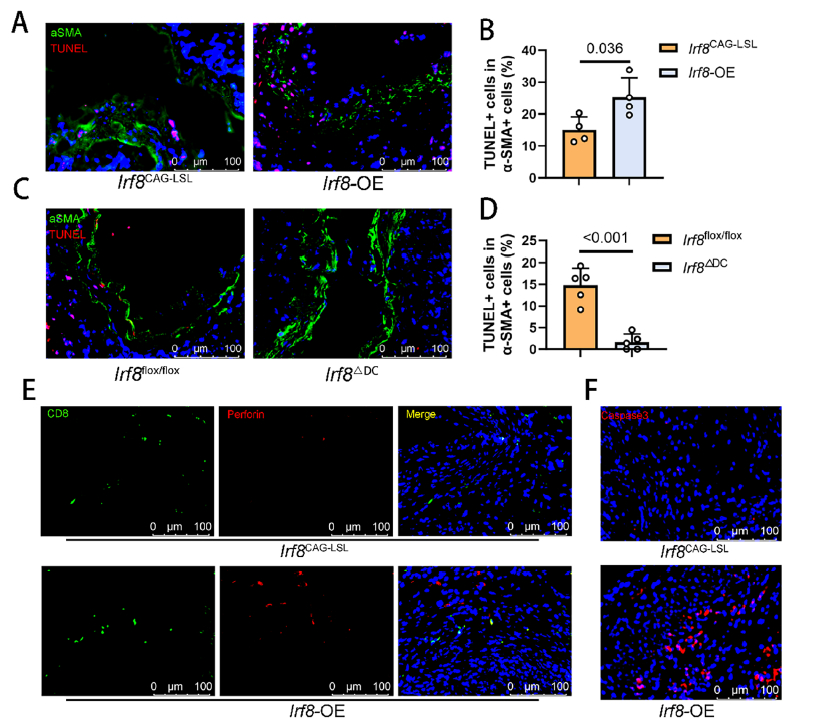
CD8+T 细胞介导主动脉平滑肌细胞凋亡(原文图 5A-F)
三、Absin 产品:关键实验的核心支撑
1. 核心产品清单
| 产品名称 | 产品货号 | 应用场景 |
|---|---|---|
| TSA 7 色试剂盒 | abs50015 | 多重免疫组化染色 |
2. 产品在研究中的关键作用
研究中,为明确 IRF8 和穿孔素(CD8+T 细胞毒性标志物)在人类 AAA 组织中的表达分布,科研团队采用了 Absin TSA 7 色试剂盒(abs50015-100T) 结合抗兔/小鼠 HRP 偶联二抗,开展多重免疫组化实验。
四、图文解析:Absin 产品助力关键结果呈现
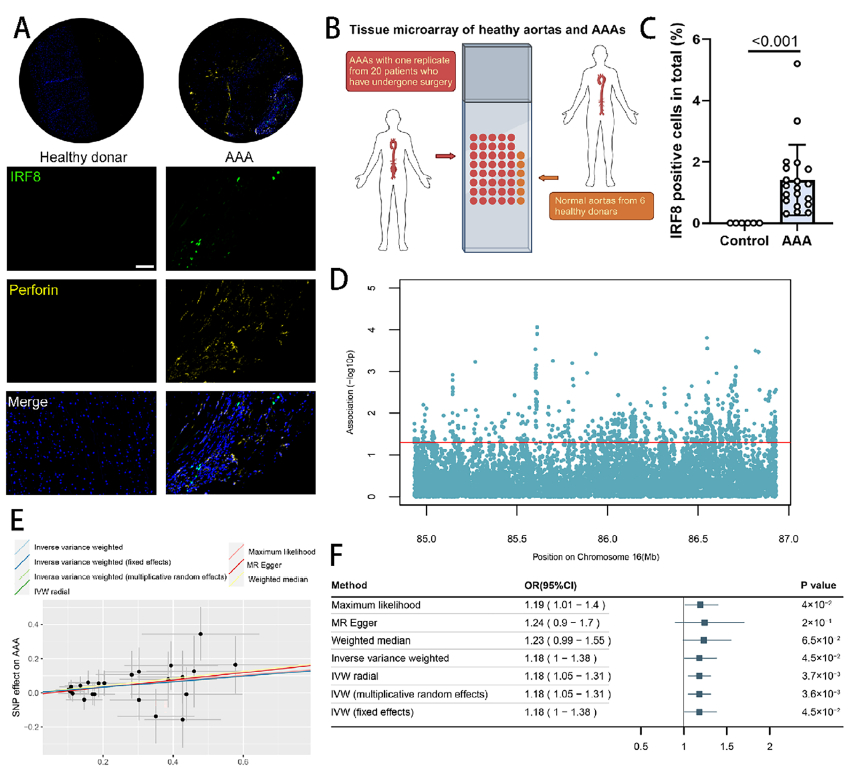
人类 AAA 组织中 IRF8 与穿孔素表达分析(原文图 7A)
如图所示,通过 Absin 多重免疫组化产品检测,科研团队直观观察到:AAA 组织中 IRF8 阳性区域与穿孔素阳性区域高度重叠,且 IRF8 表达量显著高于正常主动脉组织(P<0.001)。这一结果直接佐证了 “IRF8 通过激活 CD8+T 细胞毒性,加剧 AAA 损伤” 的核心机制,是整篇研究的关键临床数据支撑。
五、科研赋能:Absin 与科研创新同行
作为深耕生命科学领域的工具供应商,Absin 始终以 “提供高品质科研产品” 为核心,为全球科研工作者提供从免疫组化、流式细胞术到分子生物学的全流程解决方案。此次助力 AAA 领域的突破性研究,不仅体现了 Absin 产品在高灵敏度、高特异性方面的优势,更彰显了其在重大疾病机制研究中的重要价值。
未来,Absin 将持续聚焦科研痛点,迭代升级产品体系,为心血管疾病、肿瘤、免疫等领域的研究提供更高效、更精准的工具支持,与科研工作者共同探索生命科学的未知边界。
本文内容基于《Advanced Science》(DOI:10.1002/advs.202416238)原文献;文中涉及的原文献图片、数据等知识产权归原期刊及研究团队所有。若存在侵权情形,敬请及时联系我方删除,我方将积极配合处理。