- 手机:13761418683
电话:021-38015121
联系人:Absin
邮箱:zhouzz@univ-bio.com
网址:http://www.absin.cn/
地 址:上海市浦东新区新浩路58号18号楼

- 生物标志物开发:SLC25A22可作为PD-L1高表达CSCC患者免疫治疗疗效预测标志物。
- 联合治疗新策略:为免疫治疗耐药患者提供新的治疗选择,特别是PD-L1高表达人群。
- 代谢免疫治疗新方向:开辟了通过靶向肿瘤代谢增强免疫治疗效果的新途径。
突破宫颈癌免疫治疗瓶颈:靶向谷氨酰胺代谢转运体SLC25A22增强CD8+T细胞功能的新策略
2026-03-19
近日,《Advanced Science》发表重要研究,揭示了宫颈鳞癌(CSCC)中谷氨酰胺代谢异常与免疫抑制微环境的内在联系。研究发现靶向谷氨酰胺转运体SLC25A22可显著增强CD8+T细胞功能并提高抗PD-1疗法疗效。
文献标题:Targeting Glutamine Metabolism Transporter SLC25A22 Enhances CD8+ T-Cell Function and Anti-PD-1 Therapy Efficacy in Cervical Squamous Cell Carcinoma: Integrated Metabolomics, Transcriptomics and T-Cell-Incorporated Tumor Organoid Studies
发表期刊:Advanced Science(IF 14.1)
DOI:https://doi.org/10.1002/advs.202502225
使用Absin试剂:Ionomycin


一、临床痛点:宫颈癌免疫治疗响应率低的关键难题
宫颈鳞癌占宫颈癌病例的70%,传统治疗方法效果有限。尽管免疫检查点抑制剂为治疗带来新希望,但抗PD-1疗法在CSCC中的客观响应率仅为16.4%,这一临床困境亟待解决。
二、多组学整合分析揭示代谢-免疫新机制
1. 代谢组学发现谷氨酰胺代谢异常
研究团队对44例CSCC和18例正常组织进行代谢组学分析,发现2083种代谢物中,谷氨酰胺及相关代谢物在CSCC组织中显著富集。
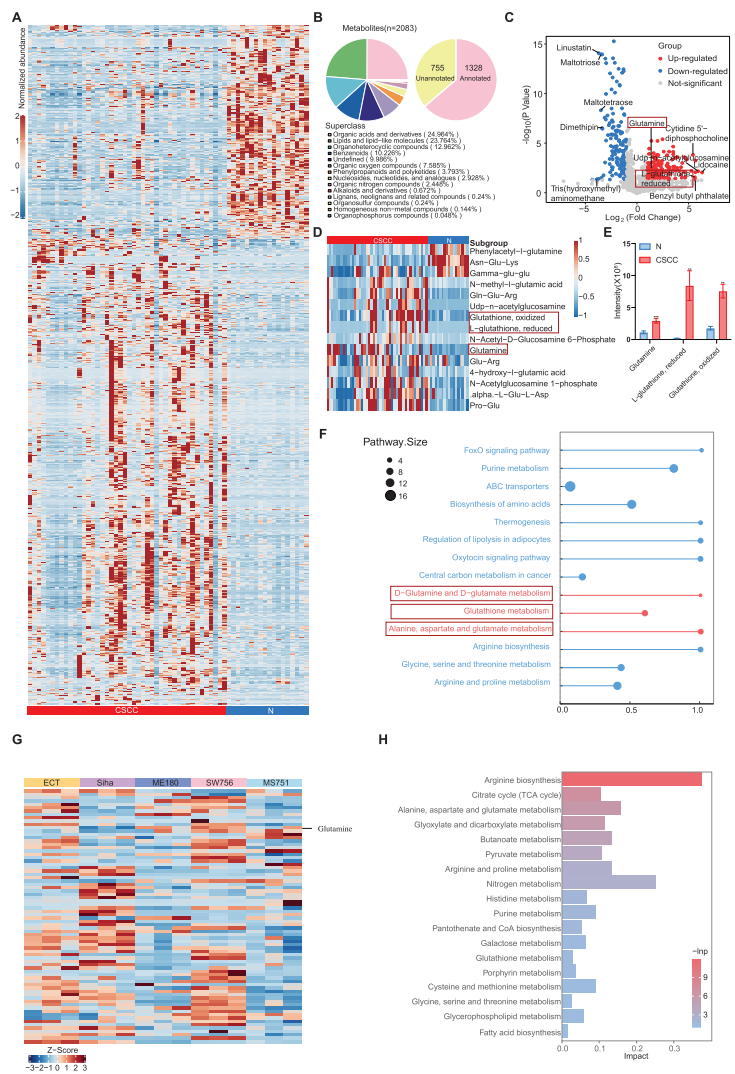
2. 转录组学证实免疫抑制微环境
转录组分析显示CSCC存在明显的免疫抑制特征,包括T细胞功能负调控通路的激活和PD-1/PD-L1信号通路的显著富集。
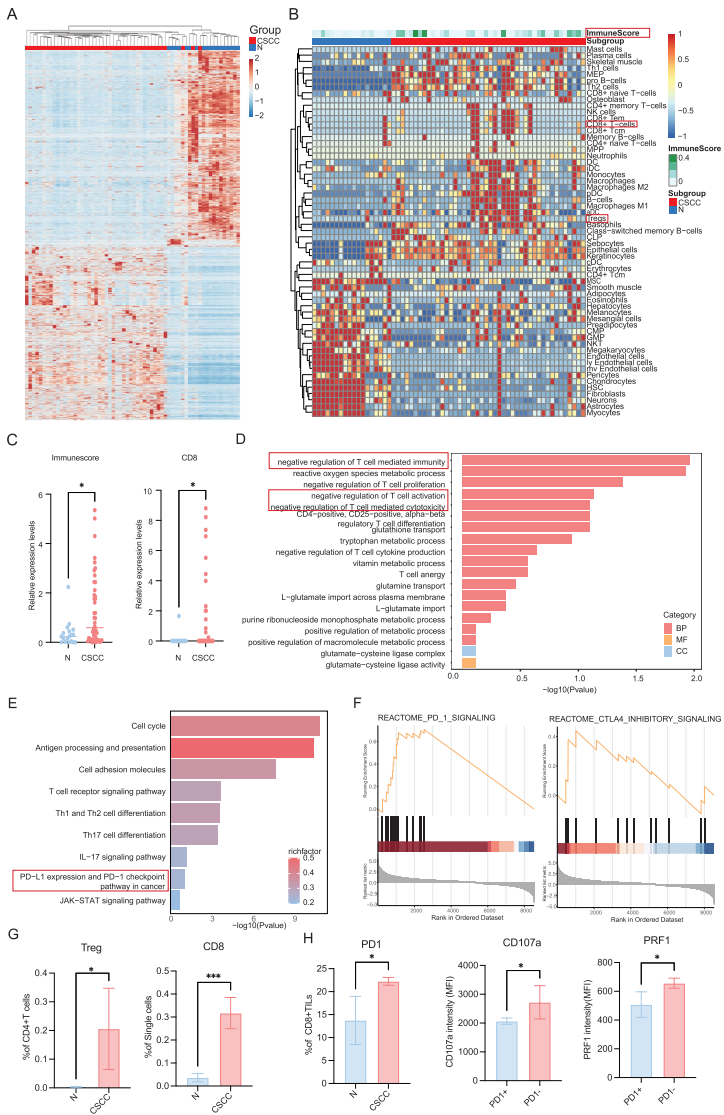
三、关键发现:SLC25A22连接代谢与免疫的桥梁
1. SLC25A22的核心作用
整合分析发现谷氨酰胺转运体SLC25A22与多个免疫检查点分子(PD-L1、CTLA-4等)呈显著正相关,成为连接代谢与免疫的关键分子。
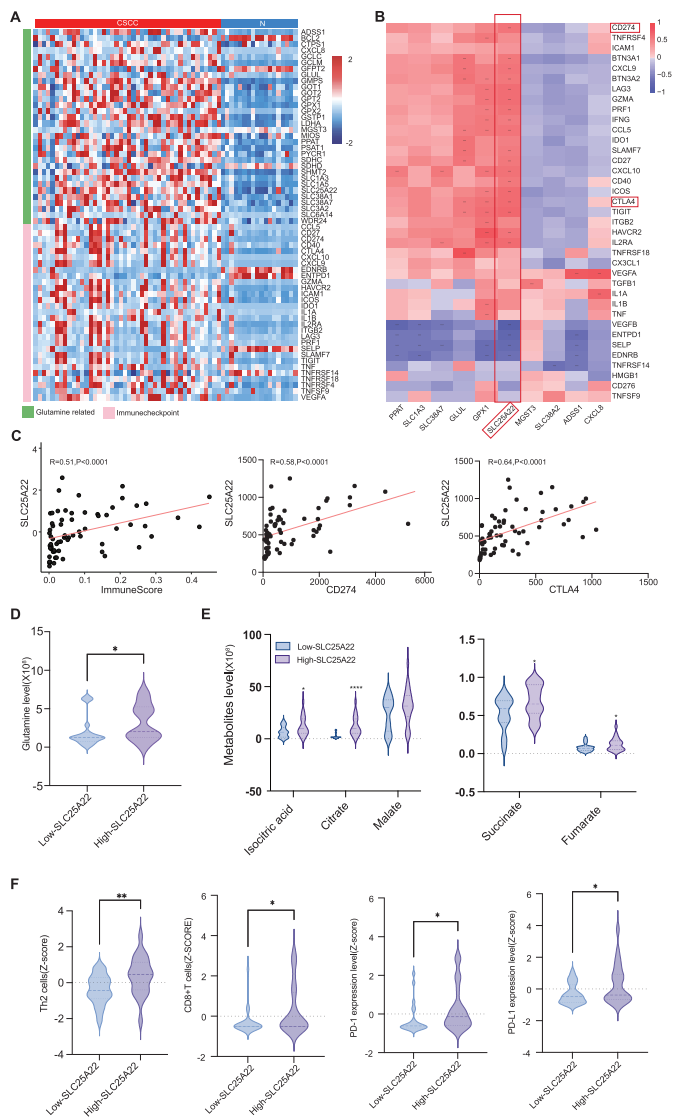
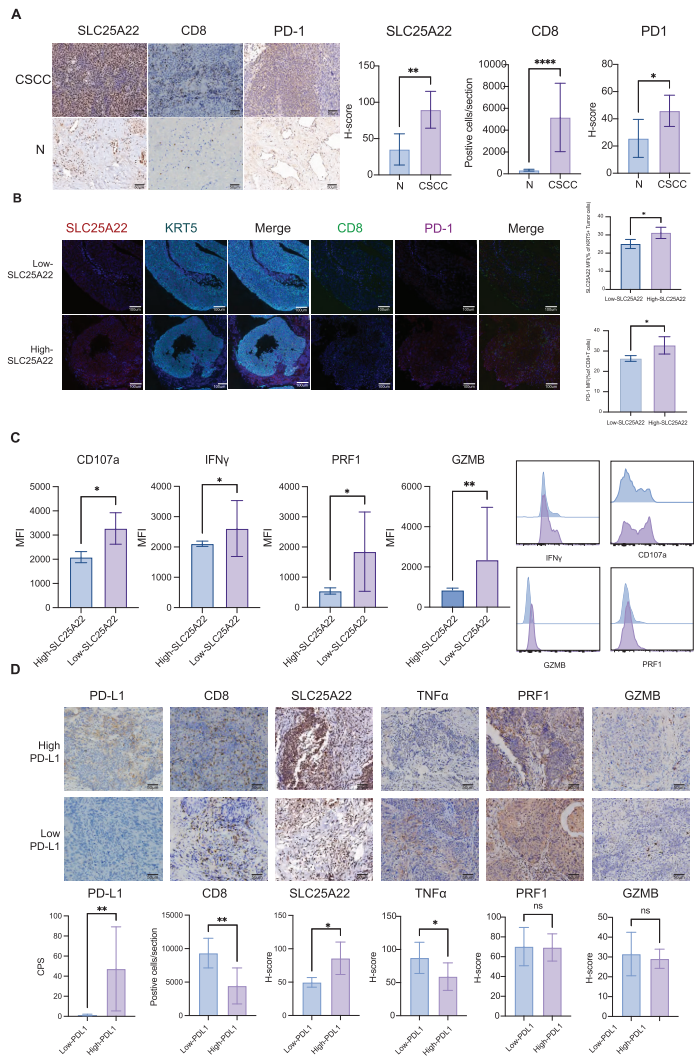
2. 临床验证证实其临床意义
在20例CSCC临床样本中验证发现,SLC25A22高表达与PD-1表达升高、CD8+T细胞毒性降低显著相关,尤其在PD-L1高表达患者中更为明显。
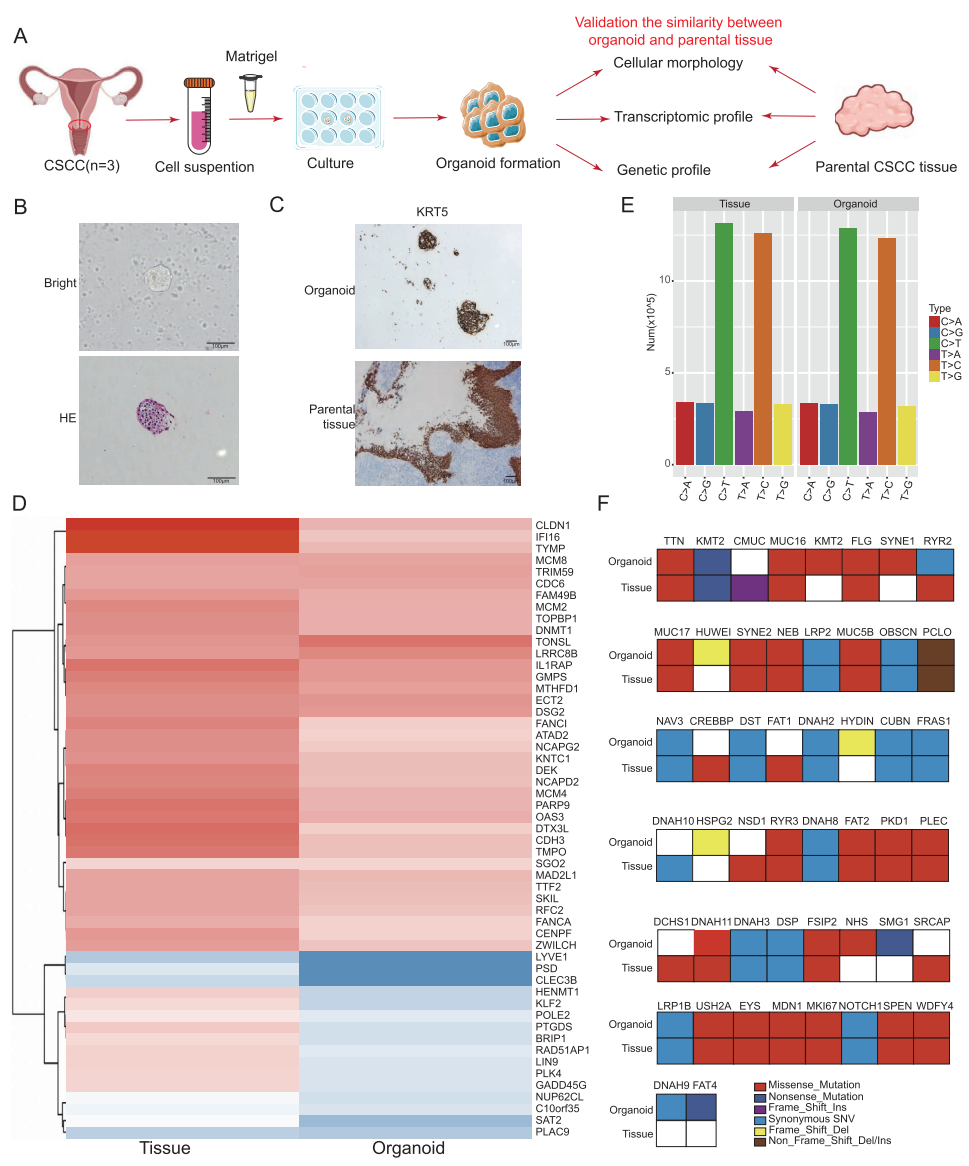
四、创新模型:3D T细胞整合类器官平台的建立
1. CSCC类器官模型的构建
成功建立保留亲代肿瘤组织学和基因组特征的CSCC类器官,为体外研究提供理想平台。
2. 3D T细胞整合类器官模型
创新性地将CD8+T细胞与肿瘤类器官共培养,真实模拟肿瘤免疫微环境中细胞间相互作用。
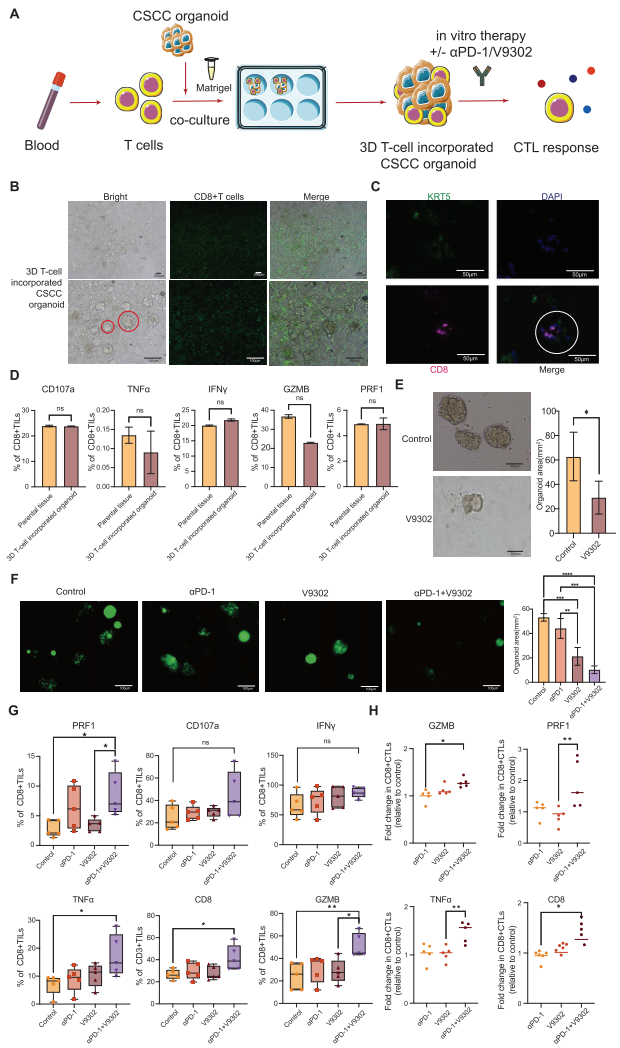
五、治疗突破:靶向SLC25A22增强免疫治疗效果
1. V-9302的有效性验证
使用谷氨酰胺转运体抑制剂V-9302靶向SLC25A22,在3D类器官模型中显著增强CD8+T细胞毒性分子(如PRF1、GZMB)表达。
2. 协同抗PD-1治疗
V-9302与抗PD-1抗体联合使用表现出显著的协同效应,显著提高治疗效果。
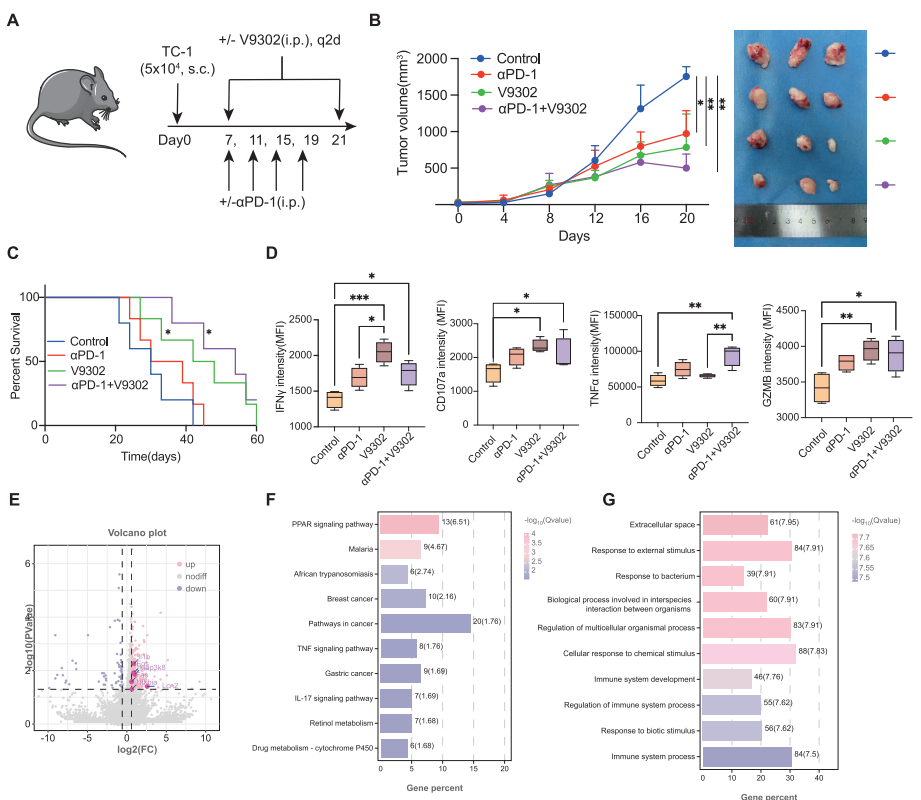
六、机制阐释:代谢重编程改善免疫微环境
1. 信号通路调控
联合治疗显著富集TNF信号通路和IL-17信号通路,激活免疫系统进程。
2. 免疫细胞功能重塑
靶向SLC25A22通过下调免疫检查点(PD-1、CTLA-4)表达,促进CD8+T细胞效应分子(IFN-γ、TNF-α、PRF1)分泌。
七、研究意义与临床转化价值
结论
本研究首次系统阐释了SLC25A22在宫颈癌免疫代谢调控中的核心作用,为克服免疫治疗耐药提供了新靶点。Absin的高质量科研试剂为这一重要发现的实现提供了可靠的技术支持。
【免责声明】本文内容基于《Advanced Science》(DOI:10.1002/advs.202502225)原文献,由 AI 解读整理;文中涉及的原文献图片、数据等知识产权归原期刊及研究团队所有。若存在侵权情形,敬请及时联系我方删除,我方将积极配合处理。