- 手机:13761418683
电话:021-38015121
联系人:Absin
邮箱:zhouzz@univ-bio.com
网址:http://www.absin.cn/
地 址:上海市浦东新区新浩路58号18号楼

- NUPR1+巨噬细胞在肿瘤组织中显著富集
- 高NUPR1表达与患者总体生存期缩短显著相关
- NUPR1特异性促进M2型巨噬细胞极化
肝癌免疫治疗耐药难题突破:乳酸化驱动NUPR1塑造免疫抑制微环境的新机制
2026-03-19
免疫治疗在肝癌中的低应答率(仅15-30%)一直是临床面临的重大挑战。《Advanced Science》上的最新研究,揭示了肿瘤相关巨噬细胞中NUPR1的作用,为克服免疫治疗耐药提供了新的解决方案。Absin的高质量重组蛋白为本研究的顺利开展提供了重要技术支持。
文献标题:Lactylation-Driven NUPR1 Promotes Immunosuppression of Tumor-Infiltrating Macrophages in Hepatocellular Carcinoma
发表期刊:Advanced Science(IF 14.1)
DOI:https://doi.org/10.1002/advs.202413095
核心产品:Recombinant Mouse CSF1 Protein(abs04383)
一、直面临床痛点:为何肝癌免疫治疗效果不佳?
肝细胞癌作为全球高发恶性肿瘤,传统治疗方法效果有限。尽管PD-1/PD-L1抑制剂在部分癌种中表现优异,但在肝癌中的应答率始终难以突破30%的瓶颈。这一临床困境的背后,是肿瘤微环境中免疫抑制性髓系细胞,特别是肿瘤相关巨噬细胞的"幕后操控"。
二、突破性发现:NUPR1——巨噬细胞中的"免疫刹车"分子
研究团队通过多组学分析,在三个独立的scRNA-seq数据集中均发现NUPR1在TAMs中特异性高表达。这一发现不仅解释了免疫抑制微环境的形成机制,更为预后预测提供了新的生物标志物。
关键证据:
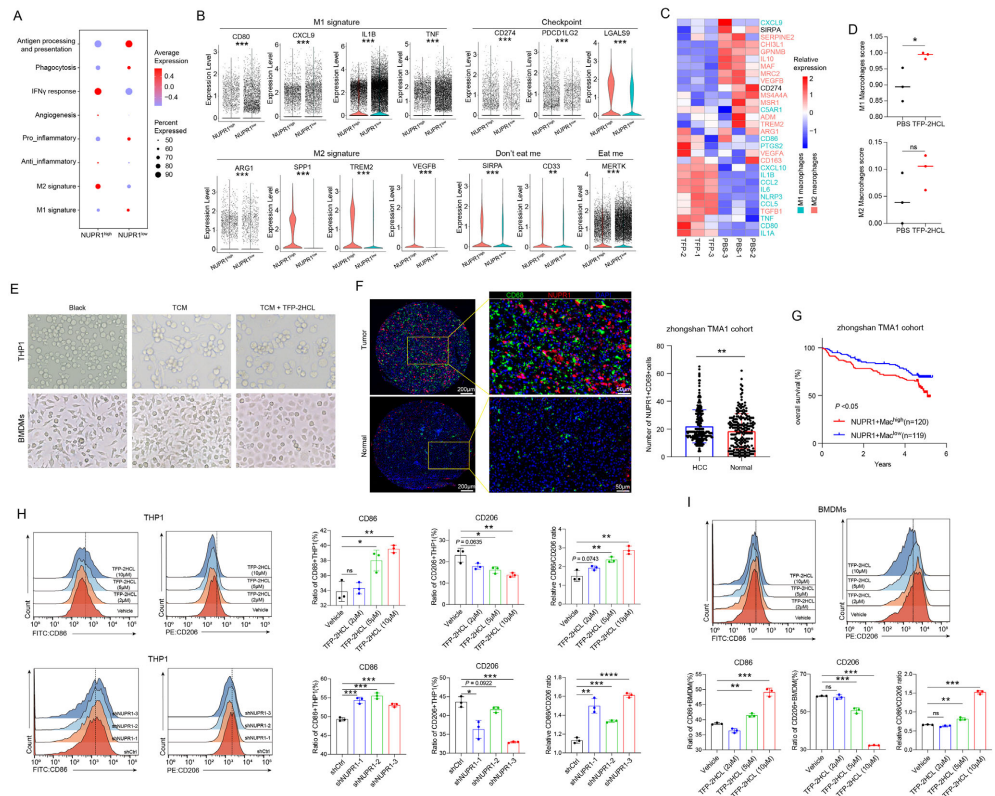
三、机制深度解析:从代谢异常到免疫抑制的完整链条
1. 信号通路层面的发现
NUPR1通过抑制ERK和JNK信号通路,促使巨噬细胞向免疫抑制性的M2表型转化。这一发现为靶向干预提供了明确的信号通路靶点。
2. 代谢调控的创新机制
肿瘤细胞通过高糖酵解产生大量乳酸,乳酸通过诱导组蛋白H3K18乳酸化修饰,直接上调NUPR1的表达,形成"代谢-表观遗传-免疫"的完整调控轴。
四、转化医学价值:从基础研究到临床应用的跨越
1. 预后预测新指标
NUPR1+巨噬细胞水平可作为肝癌患者预后的独立预测因子,为个体化治疗提供依据。
2. 联合治疗新策略
NUPR1抑制剂与PD-1抗体的联合使用,在临床前模型中显示出显著的协同抗肿瘤效果。
3. 跨癌种应用潜力
在肺癌、黑色素瘤等多个癌种中验证了NUPR1+巨噬细胞的普遍意义。
结语
本研究不仅解决了肝癌免疫治疗耐药的核心问题,更为肿瘤免疫治疗领域提供了新的研究方向。Absin很荣幸能够为这一重要突破提供优质产品,我们将继续致力于为科研工作者提供更优质的产品和服务。
【免责声明】本文内容基于《Advanced Science》(DOI:10.1002/advs.202413095)原文献,由 AI 解读整理;文中涉及的原文献图片、数据等知识产权归原期刊及研究团队所有。若存在侵权情形,敬请及时联系我方删除,我方将积极配合处理。