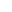- 手机:13761418683
电话:021-38015121
联系人:Absin
邮箱:zhouzz@univ-bio.com
网址:http://www.absin.cn/
地 址:上海市浦东新区新浩路58号18号楼

- 临床现象切入:再生牙髓治疗中,LPS 介导的慢性炎症常导致治疗失败,推测线粒体损伤可能是核心诱因(牙髓再生需线粒体有氧呼吸供能);
- 转录组筛选靶点:对 LPS 刺激的 DPSCs 进行转录组分析,发现阳离子稳态失调,尤其是镁离子(Mg2?)跨膜运输相关基因富集,锁定 SLC41A1(镁离子外流转运体);
- 机制深入验证:从 “Mg2?稳态失调→线粒体通透性转换孔(mPTP)开放→mtDAMPs 释放→AIM2 炎症小体激活→焦亡” 的分子路径展开验证;
- 干预策略验证:通过外源性补镁、基因沉默 / 过表达、抗体检测等手段,在细胞和动物模型中验证 “补镁逆转再生失败” 的治疗潜力;
- 标志物检测:以牙本质涎磷蛋白(DSPP)为牙髓再生核心标志物,全程追踪不同处理组的再生效果。
- 特异性强:在牙髓组织复杂背景中,可特异性识别 DSPP 蛋白,无明显非特异性染色(原文图 2C/7A/7E 均显示清晰的阳性信号定位);
- 灵敏度高:能有效检测低表达水平的 DSPP(如 LPS 组的微弱表达),准确区分不同处理组的差异;
- 兼容性好:适用于免疫组化(石蜡切片)和免疫荧光实验,满足细胞和动物水平的多场景检测需求;
- 文献背书:已被《Advanced Science》等顶刊采用,成为牙髓再生领域的信赖工具。
镁离子稳态调控机制解析:牙髓再生失败关键因素研究
2026-03-24
在再生牙髓治疗领域,慢性炎症引发的再生失败一直是临床亟待攻克的难题。近期,发表于《Advanced Science》的一项重磅研究,首次揭示了脂多糖(LPS)通过 SLC41A1 介导的镁离子外流诱发线粒体损伤和焦亡,最终导致牙髓干细胞(DPSCs)再生功能障碍的核心机制,并证实外源性补镁可有效逆转这一过程。Absin anti-DSPP 抗体(货号:abs118471)全程助力牙髓再生标志物检测,为研究成果的验证提供了可靠支撑。
文献标题:LPS-Induced Mitochondrial Damage via SLC41A1-Mediated Magnesium Ion Efflux Leads to the Pyroptosis of Dental Stem Cells
发表期刊:Advanced Science(IF 14.1)
DOI:https://doi.org/10.1002/advs.202505666
使用Absin试剂:Rabbit anti-DSPP Polyclonal Antibody(abs118471)

一、研究思路:层层递进,解锁再生失败的分子密码
该研究团队以临床痛点为切入点,构建了 “现象 - 机制 - 干预” 的完整研究链条,逻辑清晰且极具创新性:
二、核心研究成果:Mg2?稳态失衡是再生失败的关键 “绊脚石”
LPS 破坏 Mg2?稳态:LPS 激活转录因子 STAT5A,结合 SLC41A1 启动子并上调其表达,导致 DPSCs 内 Mg2?大量外流,48 小时内胞内 Mg2?含量下降约 40%;
Mg2?缺乏诱发线粒体损伤:胞内 Mg2?不足增强 CypD 与 OSCP 的结合(结合能从 - 6.8 降至 - 3.0 kcal/mol),导致 mPTP 异常开放,释放 ROS 和 mtDNA(原文图 5A/B);
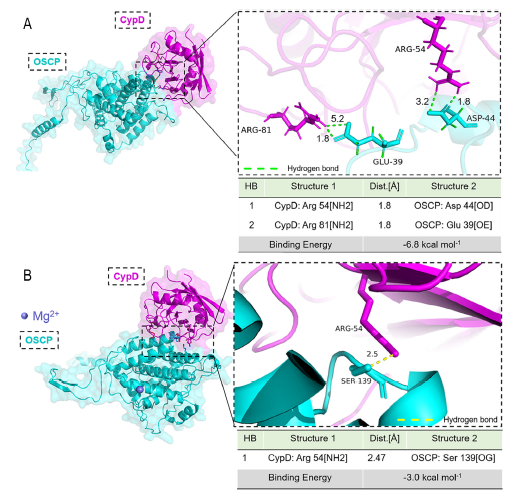
焦亡通路激活:释放的 mtDNA 激活 AIM2 炎症小体,促进 GSDMD 切割为焦亡执行片段 GSDMD-N,导致 DPSCs 焦亡(原文图 4N/P);
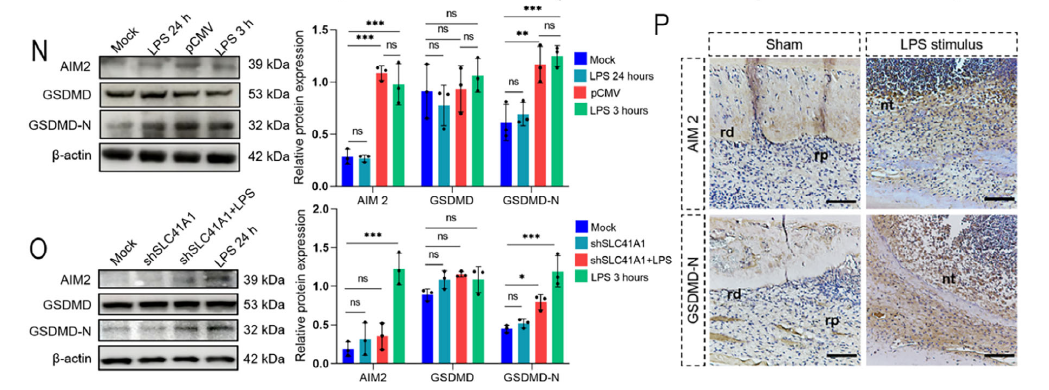
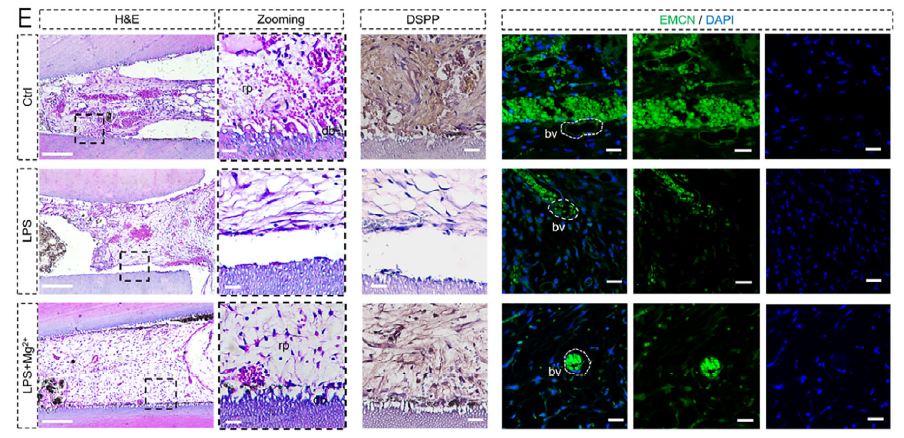
补镁逆转再生失败:外源性补充 5 mM MgCl?可恢复胞内 Mg2?稳态,抑制 mPTP 开放和焦亡,在动物模型中显著提升 DSPP 表达和牙髓样组织形成(原文图 7E)。
三、Absin 产品高光时刻:anti-DSPP 抗体(abs118471)的关键作用
| 产品名称 | 货号 | 应用实验 | 核心作用 |
|---|---|---|---|
| Anti-DSPP Antibody(牙本质涎磷蛋白抗体) | abs118471 | 免疫组化(IHC)、免疫荧光(IF) | 特异性检测 DSPP 蛋白表达,作为牙髓再生和牙本质形成的金标准标志物 |
2. 抗体在研究中的核心贡献
DSPP 是牙本质细胞分化和牙髓再生的特异性标志物,其表达水平直接反映牙髓组织的再生能力。该研究中,Absin 的 anti-DSPP 抗体贯穿细胞和动物实验的关键验证环节,为研究结论提供了直接的形态学和分子证据:
(1)验证 LPS 对再生的抑制作用(原文图 2C)
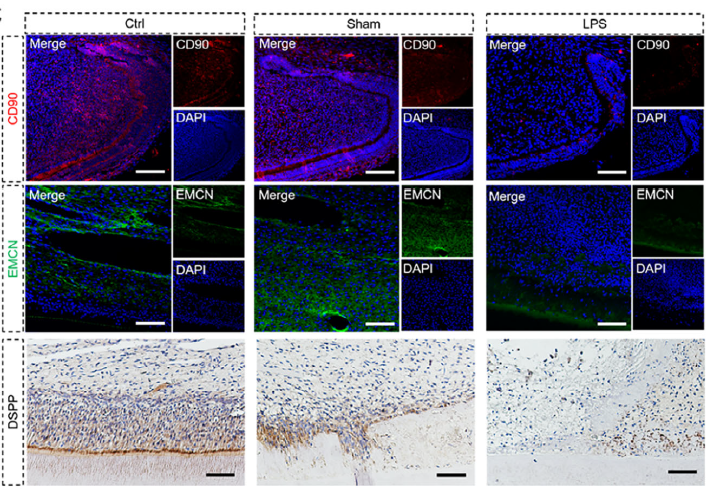
实验设计:构建大鼠切牙牙髓损伤模型,向根管内注射 LPS,3 天后通过 IHC 检测 DSPP 表达;
抗体作用:清晰显示 LPS 组牙髓组织中 DSPP 表达显著降低,且再生牙髓区域出现坏死组织(nt),证实 LPS 抑制牙本质形成和牙髓再生;
结果价值:为 “LPS 诱导再生失败” 的初始假设提供直接证据。
(2)验证镁缺乏对再生的影响(原文图 7A)
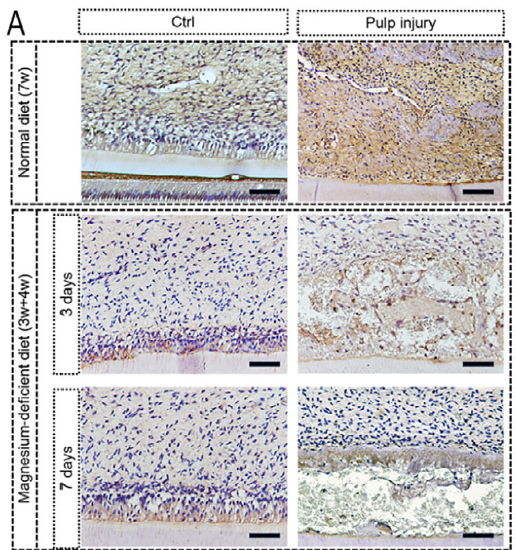
实验设计:构建镁缺乏大鼠模型,建立牙髓损伤后,通过 IHC 检测 DSPP 表达;
抗体作用:结果显示镁缺乏组再生牙髓中 DSPP 无明显上调,且存在大量坏死组织,证实 Mg2?稳态失衡本身即可抑制牙髓再生;
结果价值:明确 Mg2?稳态是牙髓再生的必要条件,为后续补镁干预提供理论依据。
(3)验证补镁的治疗效果(原文图 7E)

实验设计:构建 TDM(处理牙本质基质)皮下移植模型,分为对照组、LPS 组、LPS+Mg2?组,4 周后通过 IHC 检测 DSPP 表达;
抗体作用:清晰显示 LPS+Mg2?组 DSPP 表达显著高于 LPS 组,且再生组织与 TDM 形成牙本质小管样连接,接近正常牙髓组织的 DSPP 表达模式;
结果价值:直接证实外源性补镁可逆转 LPS 诱导的再生失败,为临床治疗提供潜在方案。
四、为什么选择 Absin 的 DSPP 抗体?
五、研究意义与产品展望
该研究不仅揭示了牙髓再生失败的全新机制,更提供了 “补镁” 这一简单有效的临床干预策略,有望推动再生牙髓治疗的规范化和成功率提升。而 Absin 的 anti-DSPP 抗体(abs118471)全程助力标志物验证,充分体现了高品质抗体对基础研究和临床转化的支撑价值。
【免责声明】本文内容基于《Advanced Science》(DOI: 10.1002/advs.202505666)原文献,由 AI 解读整理;文中涉及的原文献图片、数据等知识产权归原期刊及研究团队所有。若存在侵权情形,敬请及时联系我方删除,我方将积极配合处理。