- 手机:13761418683
电话:021-38015121
联系人:Absin
邮箱:zhouzz@univ-bio.com
网址:http://www.absin.cn/
地 址:上海市浦东新区新浩路58号18号楼

- 1. 首先通过化合物库筛选,发现 Wnt/β- 连环蛋白通路在精氨酸缺乏时对细胞存活起关键调控作用;
- 2. 利用全基因组 CRISPR 筛选和蛋白质质谱分析,锁定 SAMD4B 为 β- 连环蛋白降解的核心调控因子;
- 3. 通过精氨酸亲和探针结合互作蛋白筛选,鉴定出 BAG2 作为直接结合精氨酸的传感器;
- 4. 最终通过体外生化实验、细胞功能验证和动物模型,完整解析 BAG2-SAMD4B-β- 连环蛋白 - ATF4 的信号传导通路。
- 1. 突破抗体物种限制:支持同物种来源一抗的多重标记,无需担忧交叉反应,完美适配 BAG2 与 SAMD4B 的共定位检测;
- 2. 信号特异性强:试剂盒采用优化的荧光标记体系和信号放大技术,有效降低背景噪音,呈现清晰的蛋白定位信号;
- 3. 操作便捷高效:标准化实验流程减少操作误差,配合共聚焦显微镜可快速获取高分辨率成像结果,为机制验证提供直接视觉证据。
肿瘤细胞 “饿不死” 的秘密被破解!BAG2-SAMD4B 轴解锁精氨酸感知新机制
2026-04-20
《Molecular Cell》发表重磅研究,首次揭示 BAG2 作为精氨酸传感器,通过调控 SAMD4B-β- 连环蛋白信号通路促进肿瘤细胞在营养应激下存活的全新机制。这一发现为靶向肿瘤代谢的治疗策略提供了新靶点,而 Absin mIHC试剂盒在研究中全程助力,成为推动实验顺利开展的关键力量。
文献标题:BAG2 releases SAMD4B upon sensing of arginine deficiency to promote tumor cell survival
发表期刊:Molecular Cell(IF 16.6) | DOI:https://doi.org/10.1016/j.molcel.2025.05.035
使用 Absin 产品:四色多重荧光免疫组化染色试剂盒(鼠兔通用二抗)(abs50012)
一、研究思路:层层递进解锁精氨酸感知之谜
肿瘤细胞的快速增殖依赖充足的营养供应,精氨酸作为条件必需氨基酸,其代谢失衡与肿瘤进展密切相关。已有研究表明,部分肿瘤存在精氨酸合成酶缺陷,需依赖外源性精氨酸存活,但细胞如何感知精氨酸缺乏并启动适应性机制仍有未知。
研究团队采用 “筛选 - 验证 - 机制解析” 的递进思路:
二、核心研究成果:精氨酸感知的非经典通路
1. BAG2:全新精氨酸传感器
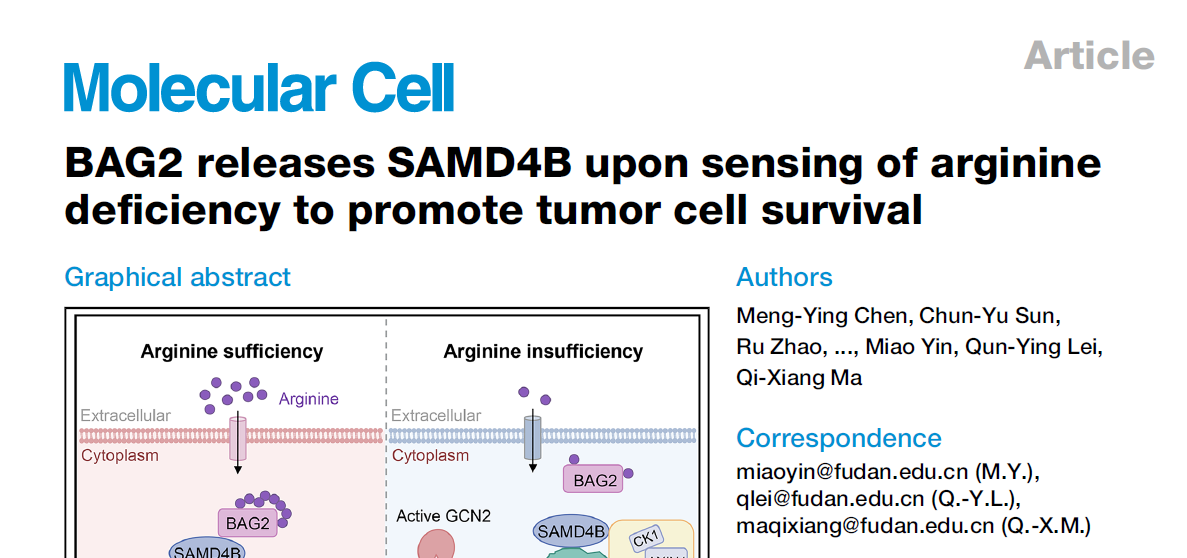
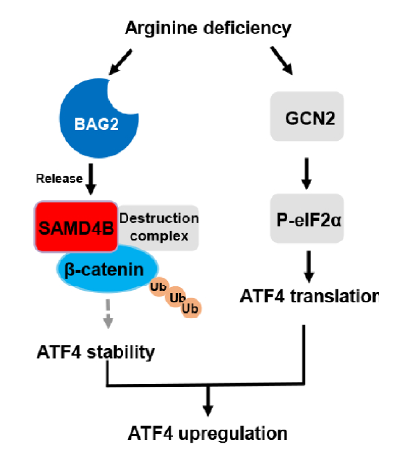
研究证实 BAG2 通过谷氨酰胺残基 Q167 直接结合精氨酸,在精氨酸充足时与 SAMD4B 紧密结合;当精氨酸缺乏时,BAG2 释放 SAMD4B,启动下游信号(图 6D)。这是首次发现 BAG2 的营养感知功能,打破了其仅作为分子伴侣调控因子的传统认知。
2. SAMD4B 介导 β- 连环蛋白降解
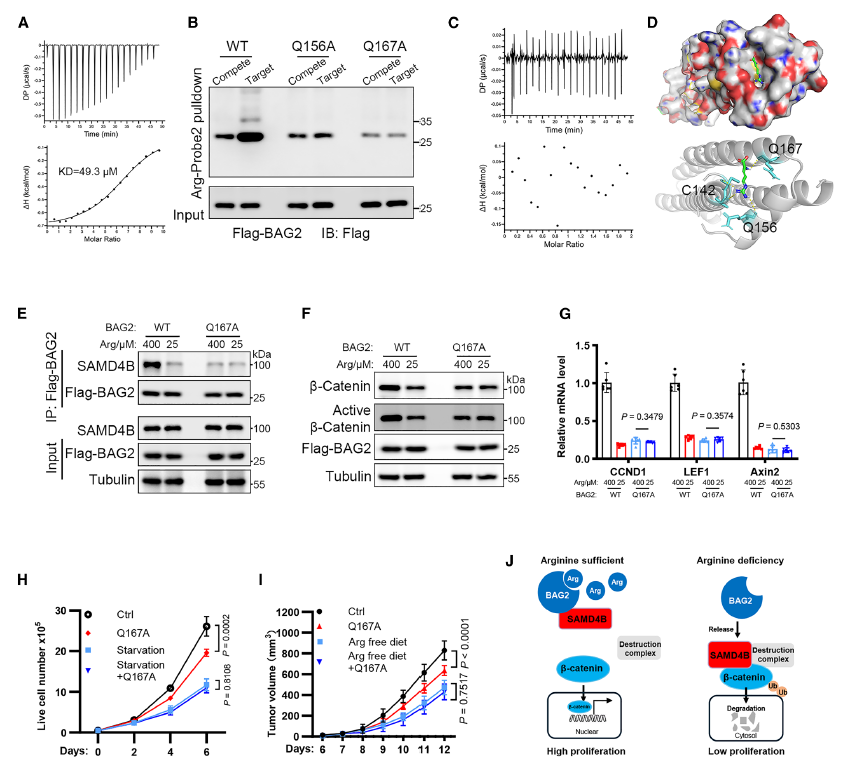
释放后的 SAMD4B 直接结合 β- 连环蛋白及降解复合物组分(CK1α、GSK3β),促进 β- 连环蛋白磷酸化和泛素化降解(图 3J、3L)。而精氨酸充足时,BAG2 对 SAMD4B 的抑制使 β- 连环蛋白稳定,激活 Wnt 通路支持细胞增殖。
3. 双通路协同调控细胞存活
精氨酸缺乏时,BAG2-SAMD4B 轴通过降解 β- 连环蛋白稳定 ATF4,与经典的 GCN2-eIF2α 通路协同激活整合应激反应(ISR),帮助肿瘤细胞适应营养匮乏环境(图 7I)。这一机制解释了为何部分肿瘤能在精氨酸剥夺治疗中产生耐药性。
三、Absin mIHC 试剂盒:实验成功的关键助力
在这项多技术交叉的研究中,Absin 的四色多重荧光免疫组化染色试剂盒(货号:abs50012)发挥了不可替代的作用,为核心机制的可视化验证提供了关键支持。
产品应用场景
| 检测指标组合 | 指标类型 | 指标功能与检测目的 |
|---|---|---|
| BAG2 + SAMD4B | 核心信号蛋白 | 1. 验证 BAG2 与 SAMD4B 的细胞内共定位区域(细胞质);2. 对比精氨酸充足 / 缺乏时,两者结合强度的动态变化 |
| DAPI | 细胞核染料 | 定位细胞核区域,排除核内信号干扰,明确 BAG2-SAMD4B 互作发生在细胞质(图 5K) |
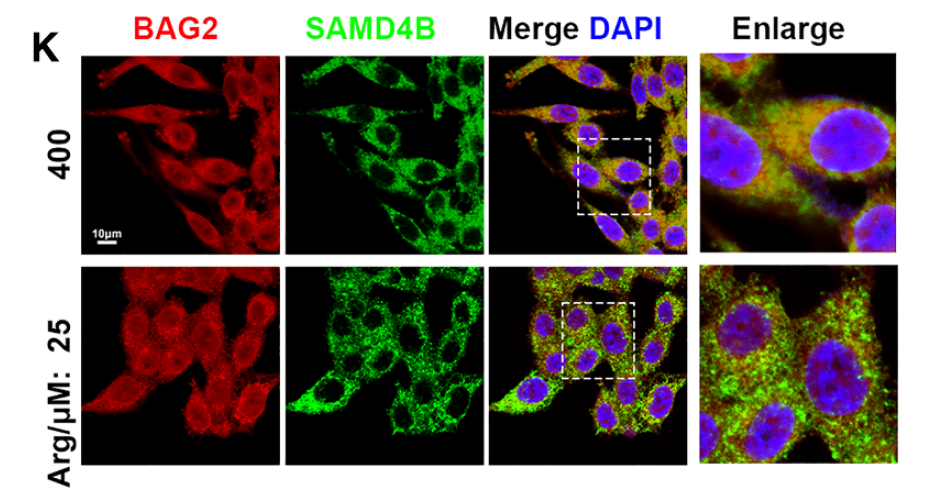
产品核心作用
四、研究意义与展望
该研究不仅揭示了精氨酸感知的非经典通路,为肿瘤代谢领域提供了全新研究方向,更对临床治疗具有重要指导意义。针对 BAG2-SAMD4B 轴的靶向干预,有望增强精氨酸剥夺疗法(如 ADI-PEG20)的抗肿瘤效果,克服耐药性难题。
Absin 始终致力于为科研人员提供高品质的实验工具,除多重免疫荧光试剂盒外,还拥有涵盖抗体、荧光探针、细胞功能检测试剂盒等在内的完整产品线,满足肿瘤学、代谢生物学等领域的多元化研究需求。未来,Absin 将持续助力更多前沿研究,为生命科学突破提供坚实支撑。
本文内容基于《Molecular Cell》(DOI: 10.1016/j.molcel.2025.05.035)原文献;文中涉及的原文献图片、数据等知识产权归原期刊及研究团队所有。若存在侵权情形,敬请及时联系我方删除,我方将积极配合处理。