- 手机:13761418683
电话:021-38015121
联系人:Absin
邮箱:zhouzz@univ-bio.com
网址:http://www.absin.cn/
地 址:上海市浦东新区新浩路58号18号楼

- 验证假设:高糖是否通过乳酸积累上调 MAD2L1,进而促进乳腺癌增殖?
- 筛选关键分子:寻找介导乳酸化修饰与 MAD2L1 调控的核心蛋白(RCC2 成为关键候选);
- 解析修饰机制:明确 RCC2 的乳酸化位点、调控其修饰的酰基转移酶;
- 探究下游通路:RCC2 乳酸化如何调控 MAD2L1 表达(SERBP1 介导的 mRNA 稳定机制);
- 验证治疗潜力:筛选靶向 RCC2 乳酸化的小分子抑制剂,评估其抗肿瘤效果。
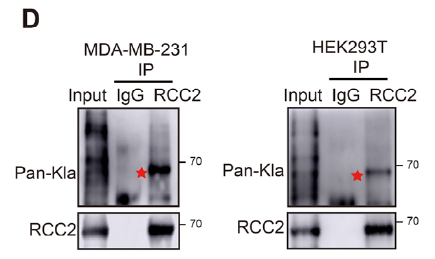
- 内源性 RCC2 乳酸化检测(图 2D):免疫沉淀 RCC2 蛋白,结合 Pan-Kla 抗体检测乳酸化水平;
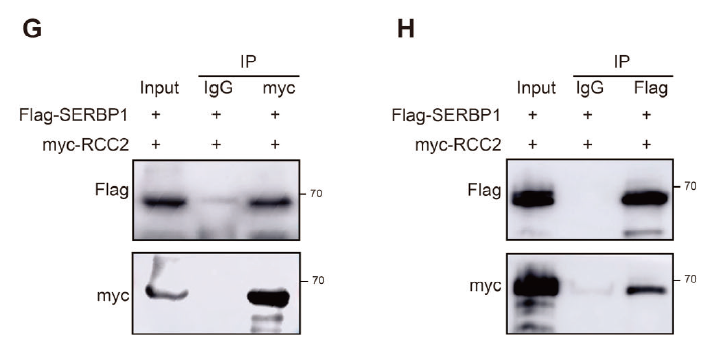
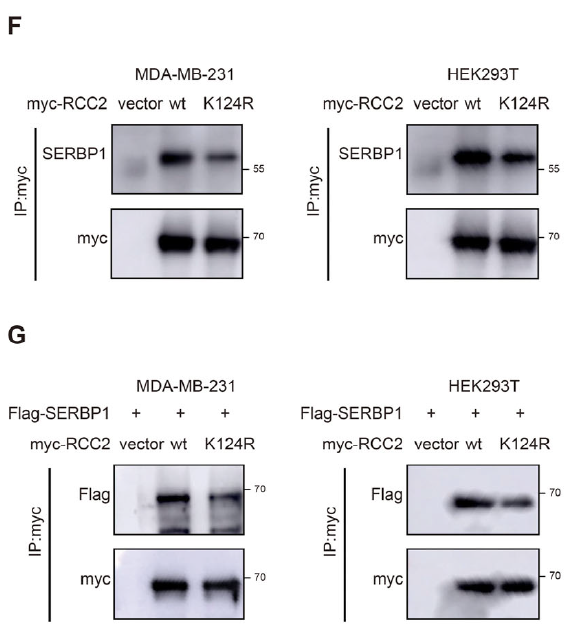
- RCC2 与 SERBP1 相互作用验证(图 4G-H、6F-G):通过 Co-IP 实验证实两者物理结合;
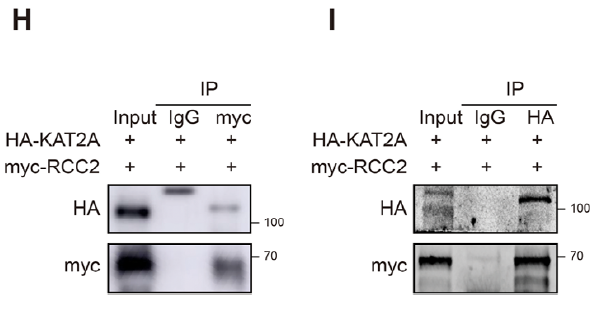
- KAT2A 与 RCC2 相互作用验证(图 3H-I):明确酰基转移酶与底物的结合关系。
高糖饮食通过诱导 RCC2 乳酸化促进乳腺癌发生发展
2026-04-20
作为女性最常见的恶性肿瘤之一,乳腺癌的发病率持续攀升,其发病机制与饮食、代谢异常的关联一直是科研热点。近期,《Advanced Science》发表的一项重磅研究,首次揭示了高糖环境下 RCC2 乳酸化修饰驱动乳腺癌增殖的核心机制,为靶向治疗提供了全新方向。而在这项突破性研究中,Absin 的明星产品全程助力,成为解析分子机制的关键工具。
文献标题:High Sugar Induced RCC2 Lactylation Drives Breast Cancer Tumorigenicity Through Upregulating MAD2L1
发表期刊:Advanced Science(IF 14.1)| DOI:https://doi.org/10.1002/advs.202415530
使用 Absin 产品:免疫(共)沉淀(IP/CoIP)试剂盒(abs955)、Organotial人乳腺癌类器官培养试剂盒(abs9446)


一、研究思路:追本溯源,破解 "高糖 - 乳酸 - 肿瘤增殖" 谜题
核心科学问题
高糖饮食已被证实与肿瘤进展相关,此前研究发现高糖可上调肿瘤组织中 MAD2L1(细胞分裂关键调控因子)的表达,但其中的分子桥梁的作用机制尚不明确。乳酸作为糖酵解的终产物,在肿瘤微环境中大量积累,且近期发现的乳酸化修饰(一种新型翻译后修饰)为代谢与信号传导的关联提供了新线索。
研究逻辑链
二、核心研究成果:四大突破,点亮乳腺癌治疗新方向
突破 1:高糖→乳酸→MAD2L1 轴是乳腺癌增殖的关键驱动
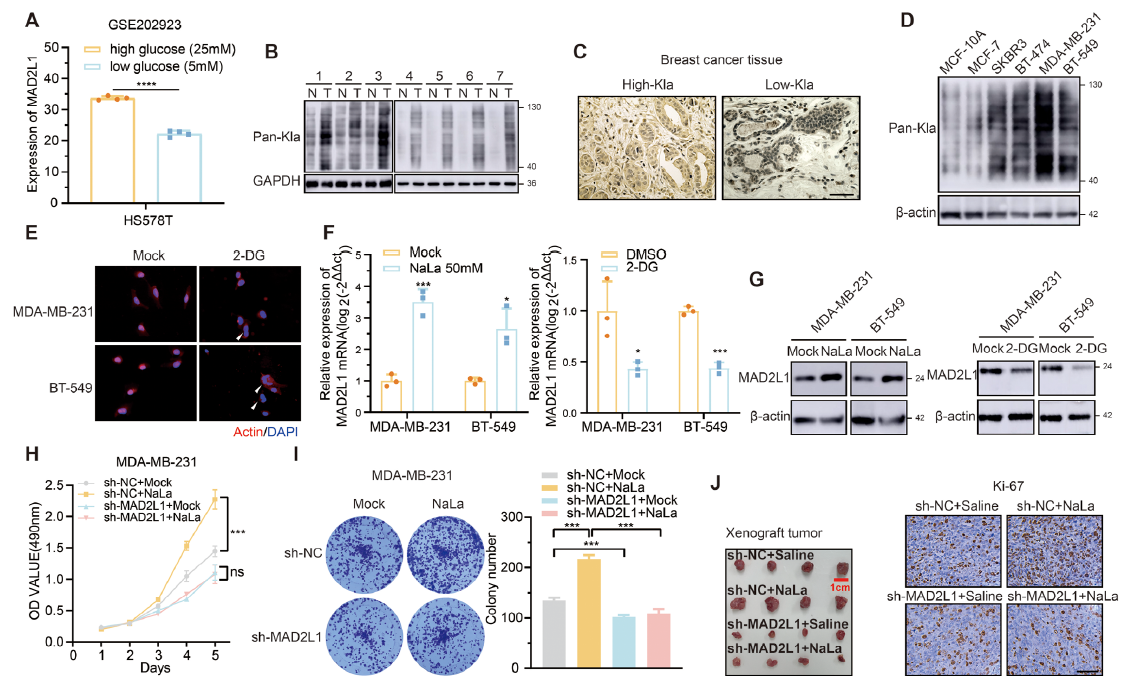
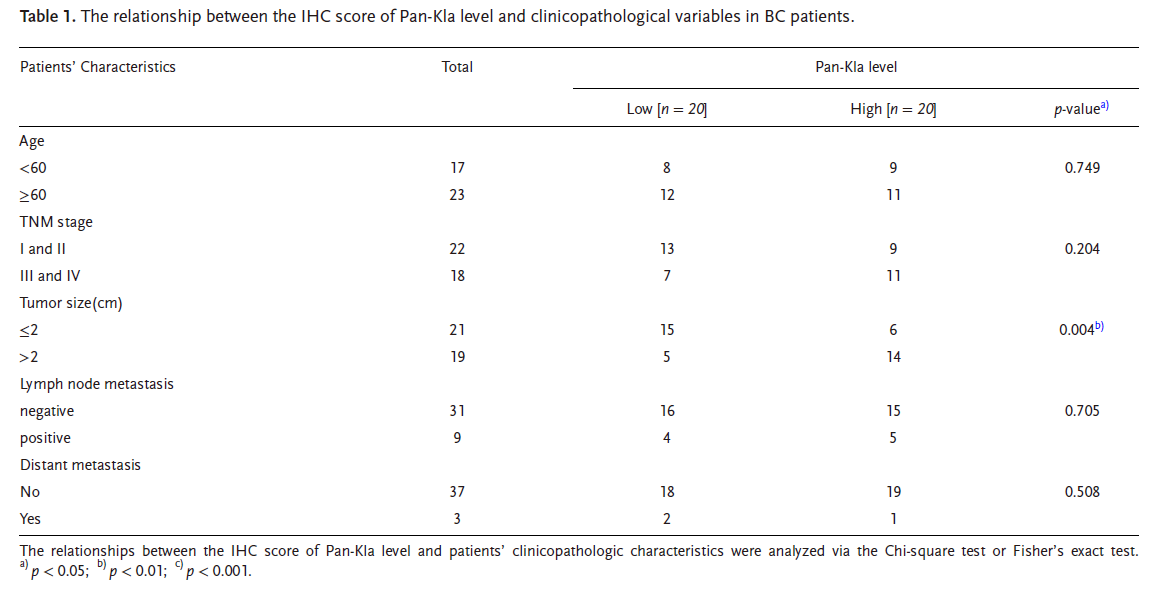
研究发现,高糖环境下乳腺癌细胞糖酵解增强,乳酸积累导致全局乳酸化水平升高(图 1B/C),且乳酸化水平与肿瘤大小显著相关(表 1)。乳酸通过上调 MAD2L1 的转录和蛋白表达,促进细胞分裂;而沉默 MAD2L1 可完全阻断乳酸诱导的肿瘤增殖(图 1H-J),证实 MAD2L1 是乳酸驱动增殖的核心下游分子。
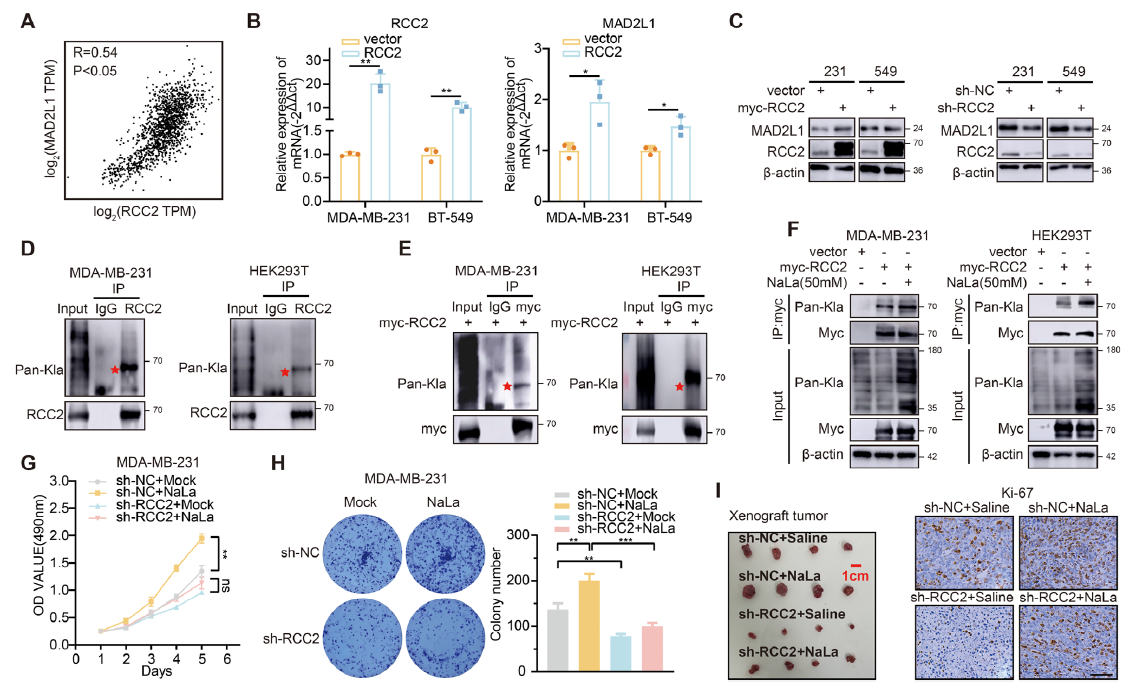
突破 2:RCC2 是乳酸化修饰的关键底物,介导 MAD2L1 上调
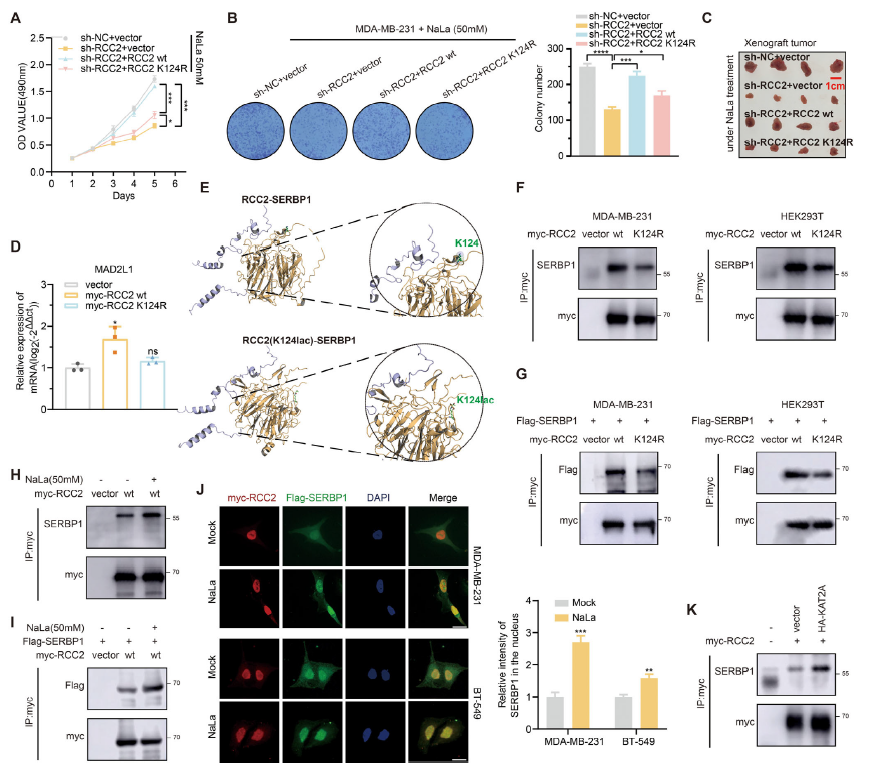
通过关联分析和免疫沉淀实验,研究首次证实 RCC2 是乳酸化修饰的底物(图 2D-E)。RCC2 与 MAD2L1 表达高度正相关,过表达 RCC2 可显著上调 MAD2L1,沉默 RCC2 则逆转乳酸诱导的 MAD2L1 表达和肿瘤增殖(图 2B-C、G-I),表明 RCC2 是连接乳酸代谢与细胞分裂的关键分子。
突破 3:KAT2A 介导 RCC2 K124 位点乳酸化,促进 SERBP1 招募
通过截短突变和质谱分析,确定 RCC2 的乳酸化位点为 K124(图 3B-C),且该位点在不同物种中高度保守(图 3E)。进一步筛选发现,酰基转移酶 KAT2A 是介导 RCC2 K124 乳酸化的关键酶(图 3F-G、K)。乳酸化修饰增强了 RCC2 与 RNA 结合蛋白 SERBP1 的相互作用(图 6F-I),促进 SERBP1 向细胞核募集(图 6J)。

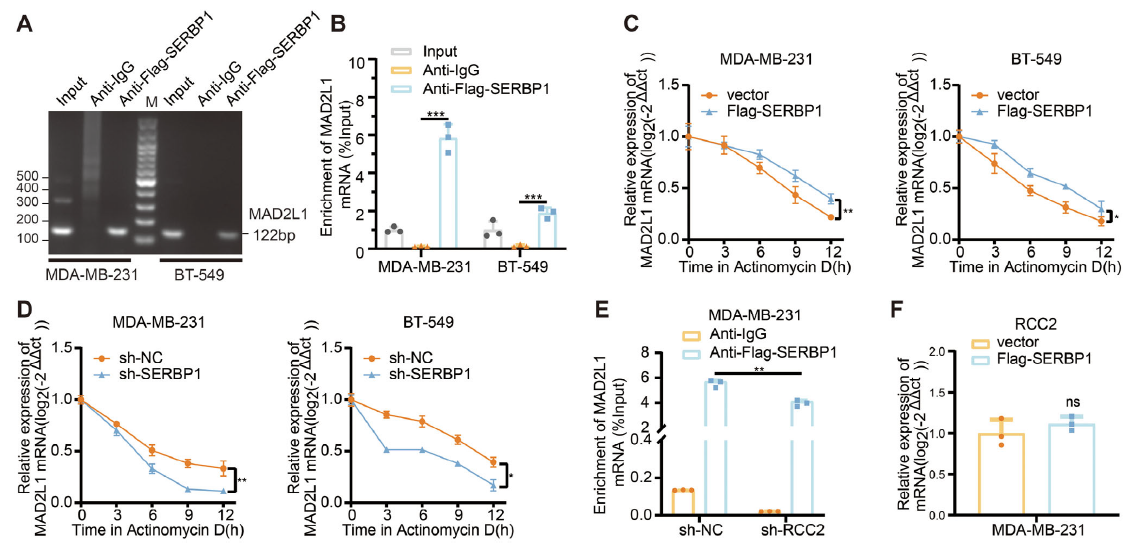
突破 4:SERBP1 结合并稳定 MAD2L1 mRNA,小分子抑制剂靶向 RCC2 乳酸化有效抑瘤
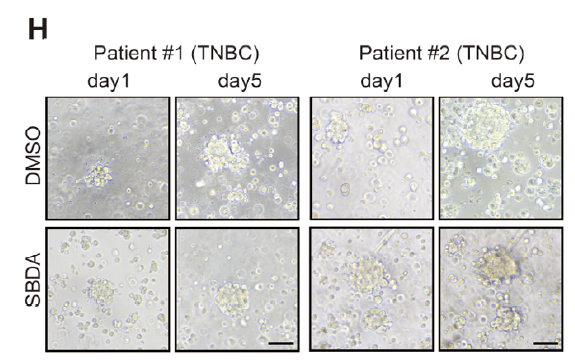
RIP 实验证实,SERBP1 直接结合 MAD2L1 mRNA 的 3'UTR 区域,延长其半衰期(图 5A-D);而 RCC2 乳酸化是 SERBP1 有效结合 MAD2L1 mRNA 的前提(图 5E)。通过虚拟筛选获得的小分子抑制剂 SBDA,可特异性结合 RCC2 K124 活性口袋,抑制其乳酸化修饰,进而下调 MAD2L1 表达,在细胞、类器官模型中均展现出显著的抗乳腺癌效果(图 7E-H)。

三、Absin 产品助力:关键实验的 "硬核支撑"
在这项机制复杂、实验设计严谨的研究中,Absin 的两款核心产品全程参与,为关键实验结果的验证提供了可靠保障:
应用场景
产品作用
作为免疫沉淀实验的核心工具,Absin 的 Protein A/G Magnetic Beads 具有高结合效率和低非特异性吸附的优势,能够高效富集目标蛋白及其结合伴侣,为乳酸化修饰检测和蛋白相互作用验证提供了高纯度的样品,确保了 Western Blot 结果的准确性和可靠性。
产品作用
类器官模型是评估药物疗效的关键临床前模型,其制备过程对细胞纯度要求极高。Absin Organotial人乳腺癌类器官培养试剂盒为 SBDA 抑制剂的类器官验证(图 7H)提供了高质量的材料。
四、总结与展望
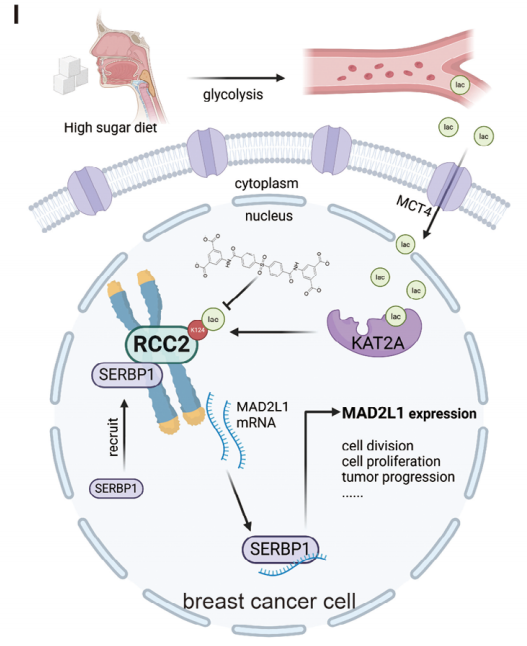
这项研究不仅揭示了 "高糖饮食→乳酸积累→KAT2A→RCC2 K124 乳酸化→SERBP1→MAD2L1 mRNA 稳定→乳腺癌增殖" 的完整调控通路(图 7I),更提出了靶向 RCC2 乳酸化的新型治疗策略,为高糖相关乳腺癌的精准治疗提供了新靶点和候选药物。
Absin 作为科研工具的可靠供应商,始终以高质量的产品支持基础医学研究。从蛋白相互作用验证到组织样本处理,Absin 的产品在关键实验环节中发挥了不可替代的作用,助力科研团队破解复杂分子机制。未来,Absin 将持续深耕生命科学研究领域,提供更多高效、精准的实验工具,支持更多突破性研究的开展,为肿瘤治疗等重大医学问题的解决贡献力量!
本文内容基于《Advanced Science》(DOI: 10.1002/advs.202415530)原文献;文中涉及的原文献图片、数据等知识产权归原期刊及研究团队所有。若存在侵权情形,敬请及时联系我方删除,我方将积极配合处理。