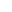- 手机:13761418683
电话:021-38015121
联系人:Absin
邮箱:zhouzz@univ-bio.com
网址:http://www.absin.cn/
地 址:上海市浦东新区新浩路58号18号楼

- 1. 通过滚环转录(RCT)技术构建含大量重复 siAkt2 序列的 RNA 微球,实现 siRNA 的高密度装载;
- 2. 经胆固醇修饰 DNA(DNA-Chol)压缩为纳米级 RNA 复合物(siAkt2 RNPs),提升细胞内化效率;
- 3. 采用生物相容性优良的 PLLA 封装形成 siAkt2 RNP@PLLA NPs,增强体液稳定性与溶酶体逃逸能力,最终实现 siAkt2 的持续胞内释放,沉默 Akt2 基因并诱导巨噬细胞 M2 极化(图 1,对应原文 Scheme 1)。
- 1. 清晰区分 M1(CD68+iNOS+)与 M2(CD68+CD163+)巨噬细胞群体,直观呈现 siAkt2 RNP@PLLA NPs 对巨噬细胞极化的调控效果;
- 2. 为 “纳米递送系统通过沉默 Akt2 诱导 M2 极化” 的核心结论提供了直接的形态学证据;
- 3. 抗体的高特异性与荧光稳定性确保了体内组织染色结果的可靠性,为后续骨再生机制分析奠定基础。
巨噬细胞 siRNA 递送 “卡脖子”?纳米系统突破降解瓶颈,点亮骨缺损修复新路径
2026-04-20
在组织再生领域,巨噬细胞的极化状态直接决定修复结局 —— 促炎 M1 表型加剧组织损伤,而促再生 M2 表型则为修复创造理想微环境。如何高效、精准地诱导巨噬细胞从 M1 向 M2 极化,一直是临床转化中的核心难题。近期发表于《Advanced Materials》的一项重磅研究,创新性地构建了 siAkt2 负载纳米递送系统,成功实现巨噬细胞代谢重编程与极化调控,为牙周炎等炎症相关骨缺损修复提供了全新策略。Absin 作为关键试剂供应商,其优质产品为该研究的顺利开展提供了坚实支撑。
文献标题:siAkt2-Loaded Nanoparticles Reprogramming Macrophages to M2 Phenotype for Effective Bone Defect Repair
发表期刊:Advanced Materials(IF 26.8) | DOI:https://doi.org/10.1002/adma.202410507
使用 Absin 产品:iNOS Antibody

一、研究思路:精准靶向 + 高效递送,破解巨噬细胞调控难题
核心痛点
siRNA 介导的基因沉默是调控细胞功能的强大工具,但巨噬细胞内丰富的核酸酶会快速降解 siRNA,且传统载体装载量有限,难以达到有效沉默阈值;同时,Akt2 激酶作为糖酵解关键调控因子,其过度激活会驱动巨噬细胞 M1 极化,加剧炎症与骨吸收。
解决方案
研究团队设计了 “多重复序列装载 + 胆固醇修饰压缩 + PLLA 封装” 的三重递送策略:
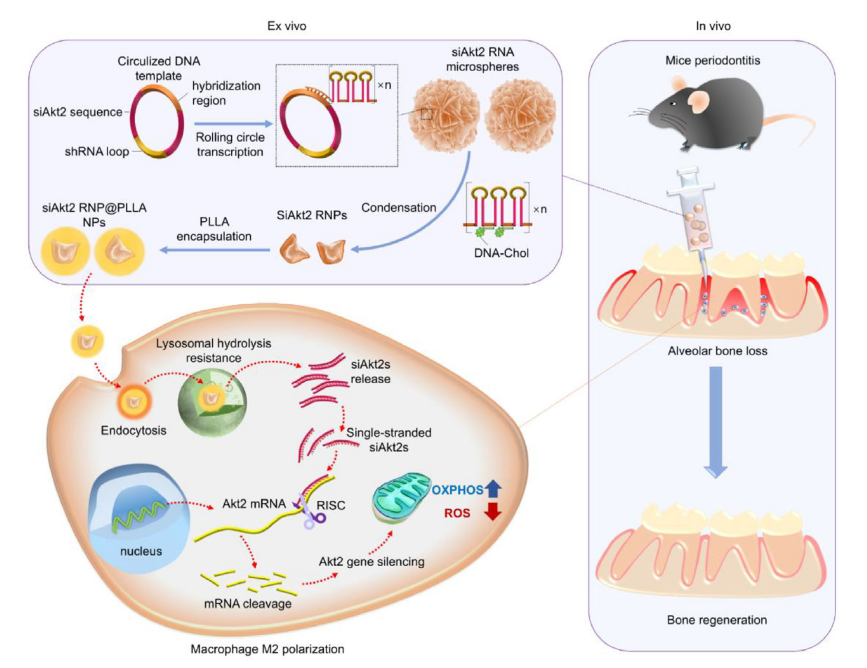
图 1 原文 Scheme 1:纳米递送系统的构建流程、胞内作用路径及骨再生机制
二、核心研究成果:从体外机制到体内修复的全链条验证
1. 纳米载体性能卓越,稳定性与递送效率双优
结构与稳定性:
siAkt2 RNP@PLLA NPs 呈清晰核壳结构,平均粒径 293.16±33.18 nm,在体液环境中 120 h 仍保持 75.85% 的完整性,且能耐受溶酶体酸性环境(图 2,对应原文 Figure 1c-e);

图 2 原文 Figure 1:a) siAkt2 微球与 RNPs 的形态;c) TEM 下 NPs 核壳结构;d) 体液中稳定性;e) 酸性环境下形态变化
胞内递送:
PLLA 外壳显著促进巨噬细胞内吞,24 h 即可实现高效溶酶体逃逸,持续释放 siAkt2,转染效率远超传统脂质体载体(图 3,对应原文 Figure 2a-b)。
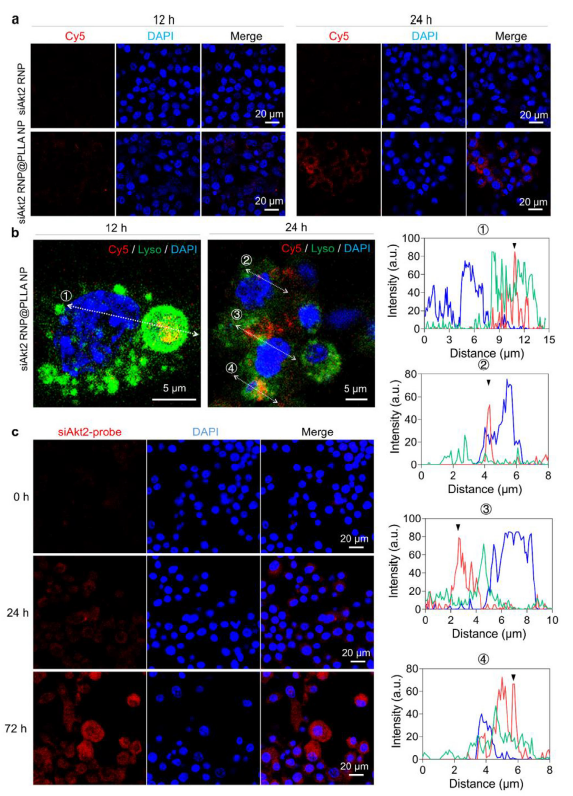
图 3 原文 Figure 2:a) 不同时间点细胞内吞效率;b) 12 h(溶酶体共定位)与 24 h(溶酶体逃逸)的荧光成像
2. 精准调控巨噬细胞功能,实现代谢重编程与 M2 极化
基因沉默效率:
qPCR 与 Western blot 证实,该系统可将 Akt2 基因表达抑制至 40-50%,且沉默效果持续 7 天以上(图 4,对应原文 Figure 3a-b);
表型转换:
显著提升 M2 标志物 CD206 的阳性率(图 4c,对应原文 Figure 3c),下调 IL-1β、TNF-α 等促炎因子,上调 IL-4、IL-10 等抗炎因子(图 4d-e,对应原文 Figure 3d-e);
代谢重编程:
抑制无氧糖酵解,增强氧化磷酸化(OXPHOS),降低 ROS 生成,修复线粒体功能(图 5,对应原文 Figure 4)。
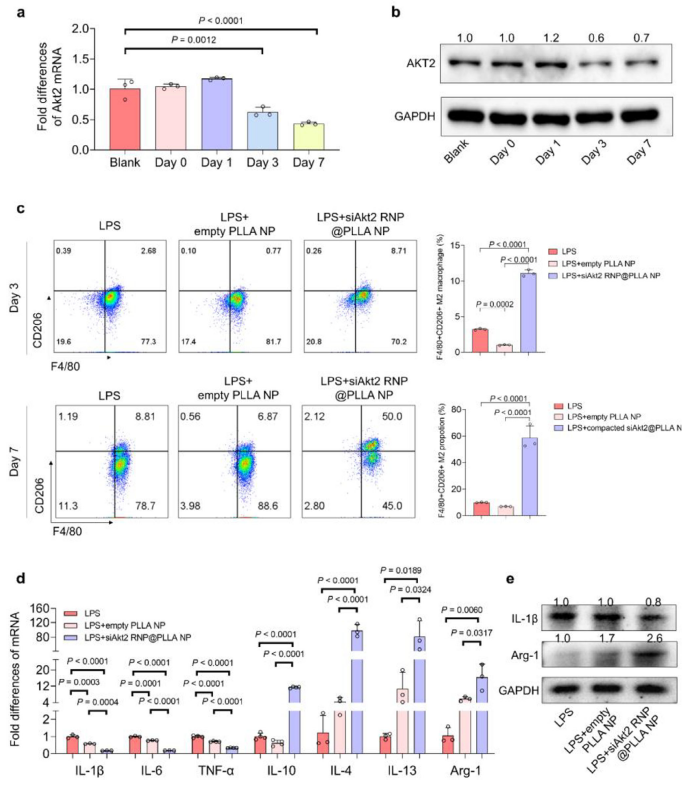
图 4 原文 Figure 3:a) Akt2 基因沉默效率;b) AKT2 蛋白表达变化;c) F4/80+CD206+ M2 细胞比例;d-e) 炎症因子表达调控

图 5 原文 Figure 4:a) 胞外酸化率(糖酵解)与耗氧率(OXPHOS);f) ROS 生成抑制;h) 线粒体膜电位修复;i) 代谢重编程机制示意图
3. 体内骨修复效果显著,临床转化潜力巨大
在小鼠牙周炎骨缺损模型中,局部注射 siAkt2 RNP@PLLA NPs 后:
骨再生能力:
4 周后牙槽骨体积分数(BV/TV)显著提升,骨缺损高度恢复至正常水平的 2/3 以上(图 6,对应原文 Figure 5d-e);

图 6 原文 Figure 5:d) 微 CT 3D 重建与骨体积分析;e) HE 染色显示骨组织再生与牙周膜形成
免疫微环境改善:
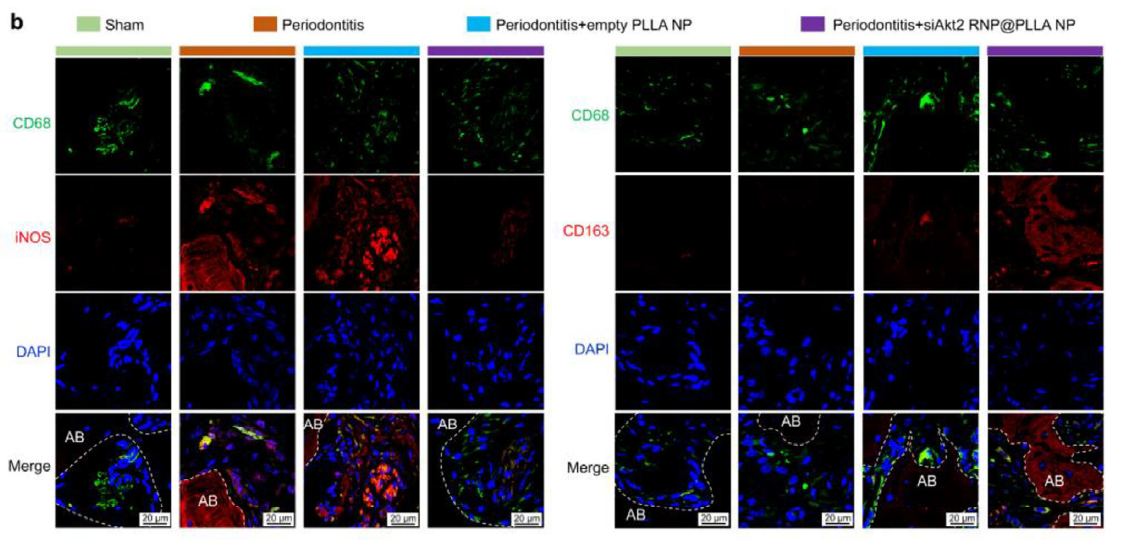
显著减少 CD68+iNOS+ M1 巨噬细胞,增加 CD68+CD163+ M2 巨噬细胞,营造促修复微环境(图 7,对应原文 Figure 6b)。
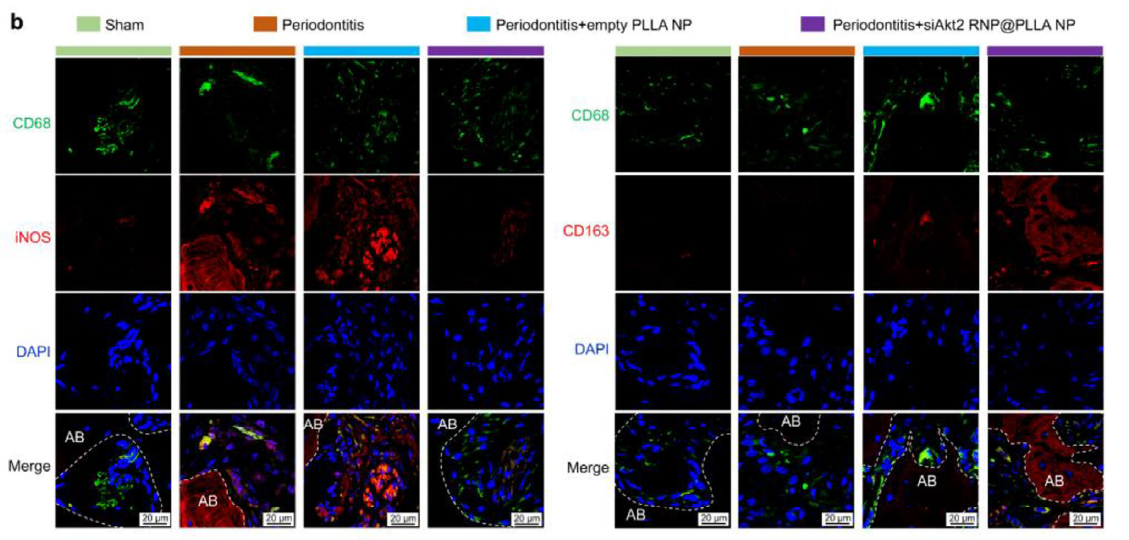
图 7 原文 Figure 6b:免疫荧光染色显示 M1(CD68+iNOS+)与 M2(CD68+CD163+)巨噬细胞比例变化
三、Absin 产品助力:关键试剂赋能研究核心环节
该研究的核心机制验证与表型分析中,Absin 的 iNOS 抗体发挥了不可或缺的作用:
产品信息
| 产品名称 | 应用场景 |
|---|---|
| iNOS Antibody | 免疫荧光染色(IF) |
核心作用
作为 M1 巨噬细胞的特异性标志物,iNOS 的表达水平直接反映促炎巨噬细胞的比例。研究中通过 Absin 的 iNOS 抗体与 CD68 抗体(巨噬细胞通用标志物)进行双重免疫荧光染色,精准量化了不同实验组中 M1 巨噬细胞的数量变化:
四、总结与展望
该研究通过创新性的纳米递送系统设计,成功突破了巨噬细胞 siRNA 递送效率低、作用时间短的技术瓶颈,为炎症相关组织修复提供了 “基因沉默 - 代谢重编程 - 免疫调控” 的一体化解决方案。Absin 的 iNOS 抗体凭借优异的特异性与适用性,成为巨噬细胞表型分析的关键工具,助力研究团队精准验证了核心机制。
未来,随着纳米递送技术与靶向治疗策略的深度融合,Absin 将持续提供高品质的免疫检测、分子生物学等系列试剂,为组织再生、肿瘤免疫、炎症调控等领域的科研创新赋能,与全球科研工作者共同推动临床转化研究的突破与发展!